
| A. |  分散系的分类 | |
| B. |  醋酸稀释 | |
| C. | 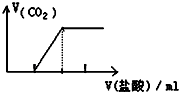 向Na2CO3溶液中逐滴滴入盐酸 | |
| D. | 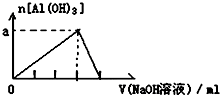 向AlCl3溶液中滴加过量的NaOH溶液 |
分析 A.分散系的本质区别是分散质微粒直径的大小;
B.溶液的导电性与溶液中离子浓度有关;
C.碳酸钠与盐酸先反应生成碳酸氢钠,碳酸氢钠再与盐酸反应生成二氧化碳;
D.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析.
解答 解:A.散系的本质区别是分散质微粒直径的大小,分散质粒度小于1nm的为溶液,大于100nm的为浊液,介于1-100nm的为胶体,故A错误;
B.醋酸溶液加水稀释溶液中离子浓度减小,溶液的导电能力逐渐减弱,故B正确;
C.碳酸钠与盐酸先反应生成碳酸氢钠,碳酸氢钠再与盐酸反应生成二氧化碳,所以开始滴加盐酸,不会产生二氧化碳,一段时间后,开始产生二氧化碳,故C正确;
D.先后发生的反应为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O,生成沉淀过程消耗的NaOH与沉淀溶解消耗的NaOH体积比是3:1,故D正确;
故选:A.
点评 本题考查了常见的用数轴法表示化学知识,难度中等,明确分散系分类依据,熟悉相关物质的性质及发生的反应是解题关键,题目难度中等.


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:选择题
| A. | CO(g)═C(s)+$\frac{1}{2}$O2(g) | B. | 2N2O5(g)═4NO2(g)+O2(g) | ||
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g) | D. | MgCO3(s)═MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不需要通过化学反应就能从海水中获得食盐和淡水 | |
| B. | 推广使用可降解塑料及布质购物袋,无法减少“白色污染” | |
| C. | 严格执行机动车尾气排入标准有利于防止大气污染 | |
| D. | 使用二氧化硫和某些含硫化合物进行增白的食品对人体健康有害 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
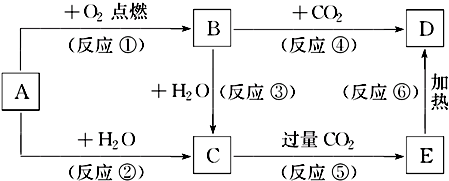
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
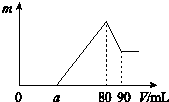 把一定质量的镁、铝混合物投入到2mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入2mol•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.
把一定质量的镁、铝混合物投入到2mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入2mol•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性KMnO4与H2C2O4溶液反应时,加入少量的MnSO4 | |
| B. | Zn与H2SO4溶液反应时,加入少的CuSO4晶体 | |
| C. | Cu 丝与浓H2SO4溶液反应时,将Cu丝做成螺旋状 | |
| D. | 铁丝能与水蒸气反应,不与冷水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品包装袋中常放入小袋还原铁粉,目的是防止食品氧化变质 | |
| B. | 铝表面有一层致密的氧化膜,故铝制容器可以用来腌制咸菜等 | |
| C. | “埃博拉”病毒在常温下较稳定,对热有中等度抵抗力,56℃不能完全灭活,60℃30min方能破坏其感染性,此过程主要发生了蛋白质的变性 | |
| D. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com