
| m |
| M |
| ���������� |
| ��Ʒ���� |
| m |
| M |
| ���������� |
| ��Ʒ���� |
| 1.496g |
| 1.64g |


 ���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
���ٴ���������ѧϰ����ѧ�ں����ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��1 | B��2��1 |
| C��1��2 | D��1��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪��E��G��Q��R��T��X��Y��Z�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵������������E�ļ��������������2�����ӣ�Gԭ���������������ڲ��������������XԪ�����������������ڲ��������ͬ��T2R�ľ������������Ӿ��壬Yԭ�ӻ�̬3pԭ�ӹ������2��δ�ɶԵ��ӣ��䵥�ʾ�����������ԭ�Ӿ��壻��Ԫ�����ڱ���ZԪ��λ�ڵ�10�У�
��֪��E��G��Q��R��T��X��Y��Z�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵������������E�ļ��������������2�����ӣ�Gԭ���������������ڲ��������������XԪ�����������������ڲ��������ͬ��T2R�ľ������������Ӿ��壬Yԭ�ӻ�̬3pԭ�ӹ������2��δ�ɶԵ��ӣ��䵥�ʾ�����������ԭ�Ӿ��壻��Ԫ�����ڱ���ZԪ��λ�ڵ�10�У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͼ��ʾ��ʵ��װ�ý���ʵ��X��Yʱ��ÿ������ӷֱ�ⶨ�ų���������������ѡ���п���ȷ��ʾʵ��X��Y�Ľ���ǣ�������
����ͼ��ʾ��ʵ��װ�ý���ʵ��X��Yʱ��ÿ������ӷֱ�ⶨ�ų���������������ѡ���п���ȷ��ʾʵ��X��Y�Ľ���ǣ�������| ʵ�� | ���õ��� |
| X | 25mL 0.2mol/L |
| Y | 50mL 0.1mol/L |
A��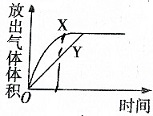 |
B�� |
C�� |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ࡢ��֬�������ʶ��ܷ���ˮ�ⷴӦ |
| B�����ࡢ��֬�������ʶ�����C��H��O����Ԫ����ɵ� |
| C�����ࡢ��֬�������ʶ��Ǹ߷��ӻ����� |
| D����֬���ͺ�֬��֮�֣��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com