
分析 Ⅰ.(1)依据热化学方程式和盖斯定律计算所需热化学方程式;
(2)①化学平衡三行计算得到平衡浓度,平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;
②当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,以此解答该题;
Ⅱ.(3)①依据平衡三行计算列式计算二氧化氮的消耗浓度,反应速率v=$\frac{△c}{△t}$;
②根据等效平衡分析;
③反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,若平衡后在A容器中再充入0.5mol N2O4,相当于增大压强平衡正向进行;
解答 解:Ⅰ.(1)①NO(g)+O3(g)?NO2(g)+O2(g)△H=-200.9kJ.mol-1
②2NO(g)+O2(g)?2NO2(g)△H=-116.2kJ.mol-1
①+②得到T℃时,反应3NO (g)+O3(g)?3NO2(g)的△H=-317.1KJ/mol,
故答案为:-317.1;
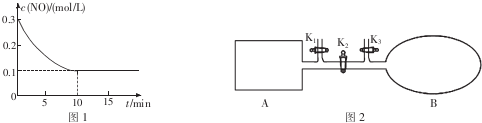
(2)①T℃时,将0.6mol NO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,图象分析可知平衡状态NO浓度为0.1mol/L,10min达到平衡,
3NO (g)+O3(g)?3NO2(g)
起始量(mol/L) 0.3 0.1 0
变化量(mol/L) 0.2 $\frac{0.2}{3}$ 0.2
平衡量(mol/L) 0.1 $\frac{0.1}{3}$ 0.2
K=$\frac{0.{2}^{3}}{0.{1}^{3}×\frac{0.1}{3}}$=240,
故答案为:240;
②反应3NO (g)+O3(g)?3NO2(g)的△H=-317.1KJ/mol,反应是气体体积减小的放热反应,
A.气体颜色不再改变,说明二氧化氮浓度不变,反应达到平衡状态,故A不符合;
B.反应前后气体质量不变,物质的量变化,当气体的平均摩尔质量不再改变说明反应达到平衡状态,故B不符合;
C.气体质量和体积不变,气体的密度始终不改变,不能说明反应达到平衡状态,故C符合;
D.反应速率之比等于化学方程式计量数之比为正反应速率之比,当单位时间内生成O3和NO2物质的量之比为1:3,表明正逆反应速率相同,反应达到平衡状态,故D不符合;
故答案为:C;
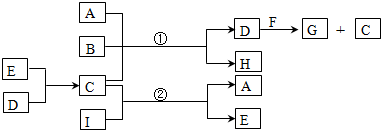
Ⅱ.(3)①关闭K2,将各1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL,若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,设生成四氧化二氮为x
2NO2(g)?N2O4(g)
起始量 1 0
变化量 2x x
平衡量 1-2x x
1-2x+x=0.8×1
x=0.2mol
则平均化学反应速率v(NO2)=$\frac{\frac{2×0.2mol}{aL}}{ts}$=$\frac{0.4}{at}$mol/(L•s),
故答案为:$\frac{0.4}{at}$mol/(L•s);
②打开K2,则相当于是在等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,
故答案为:0.7a;
③若平衡后在A容器中再充入0.5mol N2O4,相当于中等压强,平衡正向进行,则重新到达平衡后,平衡混合气中NO2的体积分数变小,故答案为:变小.
点评 本题考查热化学方程式书写、化学平衡状态的判断、化学平衡常数的计算,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意基础知识的举一反三.


科目:高中化学 来源: 题型:选择题
| A. | 3.4g H2O2中含有的共用电子对数为0.1NA | |
| B. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA | |
| C. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1 NA | |
| D. | 25℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
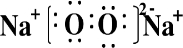 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
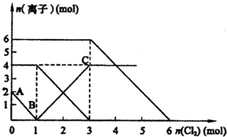 已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中,不正确的是( )
已知:2Fe2++Br2═2Fe3++2Br-、2Fe3++2I-═2Fe2++I2,向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中,不正确的是( )| A. | 还原性:Fe2+>I->Br- | |
| B. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:2:3 | |
| C. | 原混合溶液中FeBr2的物质的量为6 mol | |
| D. | 当通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “钴酞菁”分子既不能透过滤纸,又不能透过半透膜,混有氯化钠的“钴酞菁”可用渗析的方法净化 | |
| B. | “钴酞菁”与水所形成的分散系具有丁达尔效应 | |
| C. | 此项工作可以用来改变分子的某些物理性质 | |
| D. | 此项工作可广泛应用于光电器件、生物技术等方面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
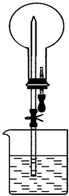 如图所示的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图所示的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A. | SO2(饱和NaHSO3溶液) 无色喷泉 | B. | NH3(H2O含酚酞) 红色喷泉 | ||
| C. | H2S(CuSO4溶液) 黑色喷泉 | D. | HCl(AgNO3溶液) 白色喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
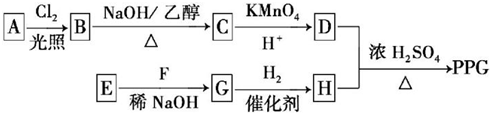
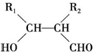 .
. .
. ,反应类型为消去反应.
,反应类型为消去反应. .
. (写结构简式);D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是c(填标号).
(写结构简式);D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是c(填标号).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com