
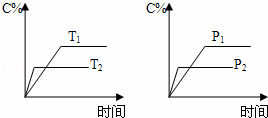
可逆反应aA(s)+bB(g)⇌cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是()
A. 达到平衡后,加入催化剂则C%增大
B. 达到平衡后,若升高温度,平衡向左移动
C. 化学方程式中b>c+d
D. 达平衡后,增加A的量,有利于平衡向右移动
考点: 体积百分含量随温度、压强变化曲线.
专题: 化学平衡专题.
分析: 可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短.由图象可知T2>T1,温度越高,平衡时C的百分含量(C%)越小,故此反应的正反应为放热反应;
当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图象可知p2>p1,压强越大,平衡时C的百分含量(C%)越小,可知正反应为气体物质的量增大的反应,即b<c+d.
A、加入催化剂同等程度增大正逆反应速率,平衡不移动;
B、温度升高,化学平衡向吸热方向移动;
C、压强越大,平衡时C的百分含量(C%)越小,可知正反应为气体物质的量增大的反应,即b<c+d;
D、A为固体,达到平衡后,增加A平衡不移动.
解答: 解:可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短.由图象可知T2>T1,温度越高,平衡时C的百分含量(C%)越小,故此反应的正反应为放热反应;
当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图象可知p2>p1,压强越大,平衡时C的百分含量(C%)越小,可知正反应为气体物质的量增大的反应,即b<c+d.
A、加入催化剂同等程度增大正逆反应速率,平衡不移动,C的百分含量C%不变,故A错误;
B、由上述分析可知,可逆反应aA(s)+bB(g)⇌c C(g)+d D(g)正反应为放热反应,升高温度平衡向吸热方向移动,即向逆反应移动,故B正确;
C、由上述分析可知,可逆反应aA(s)+bB(g)⇌c C(g)+d D(g)正反应为气体物质的量增大的反应,即b<c+d,故C错误;
D、增大固体物质的物质的量不能使平衡移动,A为固体,达到平衡后,增加A平衡不移动,故D错误.
故选B.
点评: 本题考查了体积分数随温度、压强变化曲线的分析,难度不大,明确“先拐先平数值大”是解本题的关键,注意D选项中,固体量的多少对化学平衡无影响,即不影响平衡的移动,也不影响其它气体的转化率.


科目:高中化学 来源: 题型:
根据热化学方程(在101kpa时):S(s)+O2(g)=SO2(g);H=﹣297.23kJ/mol,分析下列说法中不正确的是()
A. S的燃烧热为297.23KJ/mol
B. S(s)+O2(g)=SO2(g)放出的热量大于297.23kJ
C. S(s)+O2(g)=SO2(g)放出的热量小于297.23kJ
D. 形成1mol二氧化硫的化学键所释放的总能量大于断裂1molS和1molO2的化学键所吸收的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌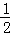 N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是()
N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是()
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下存在反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是()
A. 容器Ⅰ、Ⅱ中正反应速率相同
B. 容器Ⅰ、Ⅲ中反应的平衡常数相同
C. 容器Ⅰ中CO的物质的量比容器Ⅱ中的多
D. 容器Ⅰ中CO的物质的量比容器Ⅱ中的少
查看答案和解析>>
科目:高中化学 来源: 题型:
T℃时,有甲、乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲、乙两容器中加入6mol A和3mol B,发生反应如下:3A(g)+bB(g)⇌3C(g)+2D(g)△H<0; 4min时甲容器内的反应恰好达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L; t min时乙容器内的反应达平衡,根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)= ,化学方程式中计量数b= .
(2)乙容器中反应达到平衡时所需时间t 4min(填“大于”、“小于”或“等于”).
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是AC.
A.保持温度不变,增大甲容器的体积至2L
B.保持容器体积不变,使甲容器升高温度
C.保持容器压强和温度都不变,向甲中加入一定量的A气体
D.保持容器压强和温度都不变,向甲中加入一定量的B气体
(4)写出平衡常数表达式K= ,并计算在T℃时的化学平衡常数K .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下体积相同的下列四种溶液:①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液.下列说法中,正确的是()
A. ②和④混合,所得混合溶液的pH大于7
B. 将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>①
C. ③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④
D. ①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
在100g碳不完全燃烧所得气体中,CO占1/3体积,CO2占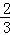 体积,且:
体积,且:
C(s)+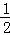 O2(g)═CO(g)△H=﹣110.35kJ;
O2(g)═CO(g)△H=﹣110.35kJ;
CO(g)+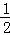 O2(g)═CO2(g)△H=﹣282.5kJ
O2(g)═CO2(g)△H=﹣282.5kJ
与这些碳完全燃烧相比,损失的热量是()
A. 392.92 kJ B. 2489.4 kJ C. 784.72 kJ D. 3274.3 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com