
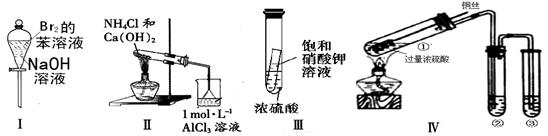
| A.实验I:振荡后静置,下层溶液颜色变深 |
| B.实验Ⅱ :烧杯中先出现白色沉淀,后溶解 |
| C.实验III:放置一段时间后,小试管内有晶体析出 |
| D.实验Ⅳ:为确认CuSO4生成,向①中加水,观察颜色 |
科目:高中化学 来源:不详 题型:单选题
| A.将AlCl3溶液蒸发结晶提取无水AlCl3 |
| B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4 |
| C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸 |
| D.将Cl2、HCl混合气体通过盛有NaHCO3饱和溶液的洗气瓶除去HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.易燃试剂应与强氧化性试剂分开放置并远离火源 |
| B.某溶液中加入盐酸,有白色沉淀生成,说明原溶液中一定存在Ag+ |
| C.用50 mL酸式滴定管可准确量取25.00 mL的KMnO4溶液 |
| D.氢氧化铁胶体加热蒸干、灼烧后有氧化铁生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验操作 | 目的 |
| A | 取绿豆大的钠分别加入到水和乙醇中 | 证明乙醇羟基中氢原子不如水分 子中氢原子活泼 |
| B | 取绿豆大的钠与钾分别投入水中 | 证明钾的金属性强于钠 |
| C | 将石蜡油在催化作用下,加强热产生的气 体通入溴的四氯化碳溶液中 | 证明产物不都是烷烃 |
| D | 蔗糖溶液加稀硫酸,水浴加热一段时间 后,加新制备的Cu(OH)2,加热 | 证明蔗糖水解后产生葡萄糖 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.少量白磷贮存在二硫化碳中 |
| B.水玻璃贮存在带玻璃塞的玻璃瓶中 |
| C.少量钠贮存在酒精中 |
| D.少量钠贮存在煤油中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
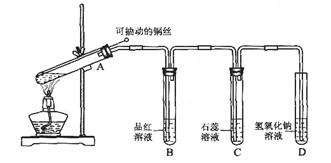
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验时,将水倒入浓硫酸配制稀硫酸 |
| B.焰色反应实验前,铂丝应先用盐酸洗净,在酒精灯外焰灼烧至没有颜色 |
| C.实验中,取用钠后的剩余部分可以放回原试剂瓶中 |
| D.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从上口倒出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com