
| A£® | ½šøÕŹÆ | B£® | øɱł | C£® | ĀČ»ÆÄĘ | D£® | Ģś |
·ÖĪö Ņ»°ćĄ“Ėµ£¬»īĘĆ½šŹōŗĶ»īĘĆ·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³ÉĄė×Ó¼ü£¬·Ē½šŹōŌŖĖŲÖ®¼äŅ׊Ī³É¹²¼Ū¼ü£¬¼ī½šŹō×唢¼īĶĮ½šŹō×åŗĶŃõ×唢Ā±×åŌŖĖŲÖ®¼äŅ׊Ī³ÉĄė×Ó¼ü£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®½šøÕŹÆĪŖŌ×Ó¾§Ģ壬C-CÖ®¼ä“ęŌŚ¹²¼Ū¼ü£¬¹ŹA“ķĪó£»
B£®øɱłĪŖ·Ö×Ó¾§Ģ壬C-OŌ×ÓÖ®¼äÖ»“ęŌŚ¹²¼Ū¼ü£¬ŹōÓŚ¹²¼Ū»ÆŗĻĪļ£¬¹ŹB“ķĪó£»
C£®ĀČ»ÆÄĘĪŖĄė×Ó¾§Ģ壬ÄĘĄė×ÓŗĶĀČĄė×ÓÖ®¼äÖ»“ęŌŚĄė×Ó¼ü£¬ĪŖĄė×Ó»ÆŗĻĪļ£¬¹ŹCÕżČ·£»
D£®ĢśĪŖ½šŹō¾§Ģ壬½šŹōŃōĄė×ÓŗĶ×ŌÓɵē×ÓÖ®¼ä“ęŌŚ½šŹō¼ü£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ¼üÅŠ¶Ļ£¬Ć÷Č·ĪļÖŹ¹¹³ÉĪ¢Į£¼°Ī¢Į£Ö®¼ä×÷ÓĆĮ¦ŹĒ½ā±¾Ģā¹Ų¼ü£¬ÖŖµĄĄė×Ó¼üŗĶ¹²¼Ū¼üµÄĒų±š£¬×¢Ņā£ŗÅäĪ»¼üŹōÓŚ¹²¼Ū¼ü£¬ĪŖŅדķµć£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę”¾Ę | B£® | ĘĻĢŃ¾Ę | C£® | °×¾Ę | D£® | »Ę¾Ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µČĪļÖŹµÄĮæÅØ¶ČµÄ°±Ė®ŗĶŃĪĖįµČĢå»ż»ģŗĻŗóµÄČÜŅŗ£ŗc£ØH+£©=c£ØOH-£©+c £ØNH3•H2O£© | |
| B£® | ÅضČĪŖ0.1mol•L-1µÄĢ¼ĖįÄĘČÜŅŗ£ŗc£ØNa+£©=2c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£© | |
| C£® | pH=12µÄ°±Ė®ČÜŅŗÓėpH=2µÄŃĪĖįµČĢå»ż»ģŗĻ£ŗc£ØCl-£©£¾c£ØNH4+£©£¾c£ØH+£©£¾c£ØOH-£© | |
| D£® | “×ĖįČÜŅŗÓėNaOHČÜŅŗĻą»ģŗĻŗó£¬ĖłµĆČÜŅŗ³ŹÖŠŠŌ£ŗc£ØNa+£©£¾c£ØCH3COO-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶ŌÓŚ0.1 mol•L-1Na2SO3ČÜŅŗ£¬ÉżøßĪĀ¶Č£¬ČÜŅŗpHŌö“ó | |
| B£® | ŌŚNH4Cl»ņAlCl3ČÜŅŗÖŠ¼ÓČėĆ¾Ģõ»į²śÉśĘųÅŻ | |
| C£® | ¾ł²»ÄܲÉČ”½«ČÜŅŗÖ±½ÓÕōøɵķ½·ØÖʵĆMgCl2”¢Al2£ØSO4£©3”¢FeCl3”¢Fe2£ØSO4£©3 | |
| D£® | ĪŖ±£“ęFeCl3ČÜŅŗ£¬ŅŖŌŚČÜŅŗÖŠ¼ÓČėÉŁĮæŃĪĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
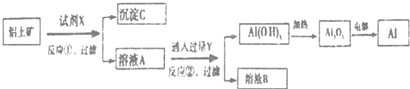
| A£® | ·“Ó¦¢ŁÖŠŹŌ¼ĮXŹĒĒāŃõ»ÆÄĘČÜŅŗ | |
| B£® | ŹŌ¼ĮYŹĒHCI£¬ĖüÓėAlO2-·“Ӧɜ³ÉĒāŃõ»ÆĀĮ | |
| C£® | Ķ¼ÖŠĖłŹ¾×Ŗ»Æ·“Ó¦ÖŠ°üŗ¬2øöŃõ»Æ»¹Ō·“Ó¦ | |
| D£® | ½«XÓėYŹŌ¼Į½ųŠŠ¶Ō»»£¬×īÖÕæÉŅŌ“ļµ½ĻąĶ¬½į¹ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2£ØHCl£©£ŗ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬Ļ“Ęų | B£® | äå±½£Øä壩£ŗĻ”NaOHČÜŅŗ£¬·ÖŅŗ | ||
| C£® | ŅŅĶé£ØŅŅĻ©£©£ŗĖįŠŌKMnO4ČÜŅŗ£¬Ļ“Ęų | D£® | ŅŅ“¼£ØŅŅĖį£©£ŗKOHČÜŅŗ£¬·ÖŅŗ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com