
| A. | 由乙醇与浓H2SO4制备乙烯;则乙烯与水反应制备乙醇 | |
| B. | 由甲苯与液溴制备邻溴甲苯;由苯制备硝基苯 | |
| C. | 由乙醛与O2制备乙酸;由乙醛与H2制备乙醇 | |
| D. | 由油酸甘油酯与H2制备硬脂酸甘油酯;由硬脂酸甘油酯制备硬脂酸 |
分析 A.由乙醇与浓H2SO4制备乙烯,生成C=C键,而乙烯与水反应制备乙醇,C=C生成C-C键;
B.苯环的H原子都被替代;
C.由乙醛与O2制备乙酸发生氧化反应;由乙醛与H2制备乙醇发生还原反应;
D.由油酸甘油酯与H2制备硬脂酸甘油酯发生加成;由硬脂酸甘油酯制备硬脂酸,发生水解反应.
解答 解:A.由乙醇与浓H2SO4制备乙烯,生成C=C键,为消去反应,而乙烯与水反应制备乙醇,C=C生成C-C键,为加成反应,故A错误;
B.苯环的H原子都被替代,都为取代反应,故B正确;
C.由乙醛与O2制备乙酸发生氧化反应;由乙醛与H2制备乙醇发生还原反应,反应类型不同,故C错误;
D.由油酸甘油酯与H2制备硬脂酸甘油酯发生加成;由硬脂酸甘油酯制备硬脂酸,发生水解反应,故D错误.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物中的官能团及官能团与性质的关系为解答的关键,侧重性质及有机反应类型的考查,题目难度不大.


科目:高中化学 来源: 题型:推断题
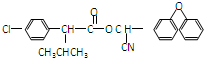 )
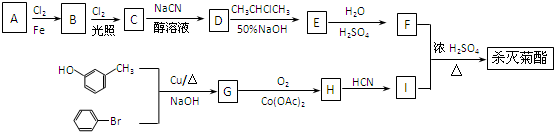
)
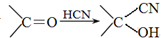
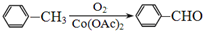
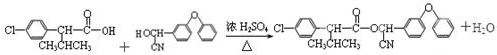 .
.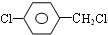 +3NaOH$\stackrel{高温高压}{→}$2NaCl+H2O+
+3NaOH$\stackrel{高温高压}{→}$2NaCl+H2O+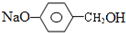
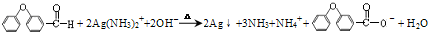
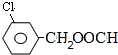 、
、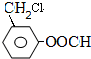 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若每消耗2n mol HI的同时生成n mol H2,表明该反应已达平衡 | |
| B. | 容器内的压强不发生变化,表明该反应已达平衡 | |
| C. | 平衡时,若其他条件不变,再充入一定量HI,重新达平衡后,I2的百分含量增大 | |
| D. | 平衡时,若其他条件不变,升高温度,混合气体的颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m-13=n | B. | n+5=m | C. | m+8=n | D. | n-11=m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中可以同时含有Fe2+、NO3- | B. | 溶液中一定有OH-、Na+ | ||
| C. | 溶液中可能含有Na+、H+、Mg2+、NO3- | D. | 若X是AlO2-,则上述离子最多有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | Ⅲ |
| ② | 制备二氧化硫 | Na2SO3→SO2 | Ⅲ |
| ③ | 制备氯气 | HCl→Cl2 | Ⅰ或Ⅲ |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
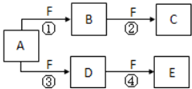 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示:
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:Z>Y>X>W | |
| B. | X、Y、Z、W 形成的单质最多有 6 种 | |
| C. | X 元素最高价氧化物对应水化物的化学式为:H3XO4 | |
| D. | 四种元素的气态氢化物中,W 的气态氢化物最稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同温度下,pH=1且体积为1L的硫酸溶液所含的H+数与pH=13且体积为1L的氢氧化钠溶液所含的OH-数一定均为0.1NA | |
| B. | 7.8gNa2S和Na2O2的混合物中所含离子数为0.3NA | |
| C. | 在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2,转移的电子数为8NA | |
| D. | 在标准状况下,2.24LHF中含有的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com