
| A. | 下列物质的沸点按由低到高的顺序排列为CH3(CH2)2CH3<CH3(CH2)3CH3<(CH3)3CCH3<(CH3)2CHCH2CH3 | |
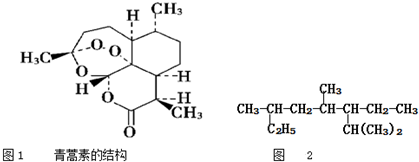
| B. | 青蒿素是抗疟疾特效药,结构如图1所示,有酯基、过氧键和醚键,不溶于水,易溶于氯仿、丙酮等,可以用乙醚从植物中提取,能够发生水解反应,具有强氧化性 | |
| C. | 油脂在一定条件下水解成高级脂肪酸和甘油,称为皂化反应 | |
| D. | 按系统命名法命名时,图2有机物的名称是3,5,7-三甲基-6-乙基辛烷 |
分析 A.烷烃随着分子中碳原子数的递增呈规律性变化,沸点逐渐升高,碳原子数相同的烃,支链越多,熔、沸点越低;
B.由结构图可知青蒿素含有的官能团,根据官能团判断青蒿素的性质;
C.油脂碱性条件下水解成高级脂肪酸盐和甘油,称为皂化反应;
D.从靠近支链的一端开始编号,2、4、6号C上分别有一个甲基,3号C上有一个乙基.
解答 解:A.烷烃随着分子中碳原子数的递增呈规律性变化,沸点逐渐升高,碳原子数相同的烃,支链越多,熔、沸点越低,因此沸点为CH3(CH2)2CH3<(CH3)3CCH3<(CH3)2CHCH2CH3<CH3(CH2)3CH3,故A错误;
B.由青蒿素的结构图可知,含有酯基、过氧键和醚键,不含羧基和羟基,不溶于水,易溶于有机溶剂,酯基能发生水解反应,过氧键具有氢氧化性,故B正确;
C.油脂碱性条件下水解成高级脂肪酸盐和甘油,称为皂化反应,故C错误;
D.按系统命名法命名时,图2有机物的名称是2,4,6-三甲基-3-乙基辛烷,故D错误;
故选B.
点评 本题考查烷烃的命名及性质规律、青蒿素的结构和性质推断、油脂的性质,综合性较强,其中B选项是高考的热点,题目难度中等.


科目:高中化学 来源: 题型:解答题
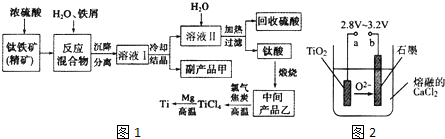
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-14 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质 | |
| B. | 人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 | |
| C. | 长期烧水的水壶内壁容易形成一层水垢,可以用食醋除去 | |
| D. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
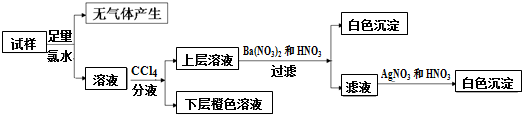
| A. | 若步骤中Ba(NO3)2和HNO3溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响 | |
| B. | 无法确定原溶液中是否存在Cl- | |
| C. | 肯定存在的离子是SO32-、Br-,是否存在Na+、K+需要通过焰色反应来确定 | |
| D. | 肯定不存在的离子是Mg2+、Cu2+、SO42-、CO32-,是否含NH4+另需实验验证 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH(CH2CH3)2的系统命名为3-甲基戊烷,与CH3CH2CH(CH3)CH2CH3互为同系物 | |
| B. | 乙烯、氯乙烯和聚氯乙烯都能因发生加成反应而使溴水褪色 | |
| C. | 用甘氨酸(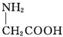 )和丙氨酸( )和丙氨酸(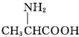 )的混合物在一定条件下可形成四种链状二肽 )的混合物在一定条件下可形成四种链状二肽 | |
| D. | 甲苯(C7H8)和甘油(C3H8O3)混合物,当总质量一定时,随$\frac{n({C}_{7}{H}_{8})}{n({C}_{3}{H}_{8}{O}_{3})}$比值增大,耗氧量和生成水的量都增大. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离Fe2O3、Al2O3操作依次为溶解、过滤、灼烧 | |
| B. | 粗盐可通过溶解、过滤、蒸发、结晶的方法提纯 | |
| C. | 配制氯化铁溶液,是将FeCl3溶于蒸馏水,再加入一定量的铁粉 | |
| D. | 取用金属钠或钾时,没用完的钠或钾要放回原瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,Z的原子序数为24.
原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,Z的原子序数为24.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
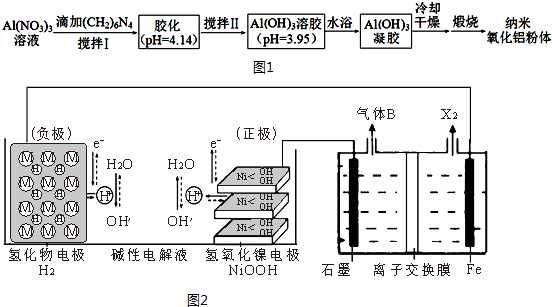
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com