
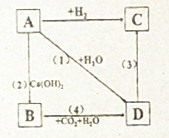
 某学生做了一系列有关氯元素单质及其化合物的实验.
某学生做了一系列有关氯元素单质及其化合物的实验.
| ||
| ||


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
| A、6.72L | B、4.48L |
| C、3.36L | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类、油脂、蛋白质完全燃烧只生成CO2 和H2O |
| B、丁烷(C4H10)和二氯甲烷都存在同分异构体 |
| C、向溴水中加入苯,振荡静置后观察下层几乎无色 |
| D、汽油、柴油、植物油都是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
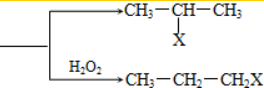
 的香料物质.
的香料物质.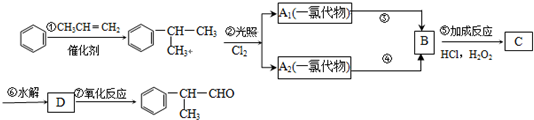
查看答案和解析>>
科目:高中化学 来源: 题型:
| 名称 | 化学式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) |
| 草酸 | H2C2O4 | - | 易溶于水 | 189.5 | 1.900 |
| 草酸晶体 | H2C2O4?2H2O | 无色晶体 | - | 101.5 | 1.650 |
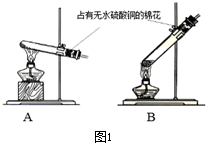
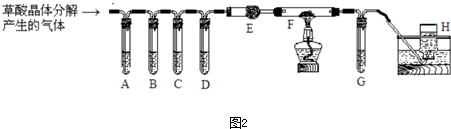
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 向5%的H2O2溶液中滴入FeCl3或CuSO4溶液时都有细小气泡产生,滴入FeCl3溶液产生的气泡更快些. | 证明催化剂有选择性 |
| B | 红砖样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | 检验红砖中的红色物质是否是Fe2O3 |
| C | 将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,反复多次 | 验证乙醇能否被氧化为乙醛 |
| D | 先将FeCl3固体溶于较浓盐酸,再加水稀释 | 配制FeCl3溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7:1 | B、7:2 |
| C、7:3 | D、7:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com