
在硫酸的工业制法中,你认为下列生产操作与说明生产操作的重要原因都正确的是
[ ]
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能在空气中燃烧
B.硫铁矿燃烧得到的气体混合物需净化,因为其中的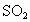 会与杂质反应
会与杂质反应
C.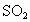 氧化为
氧化为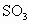 需使用催化剂,因为没有催化剂
需使用催化剂,因为没有催化剂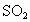 不能与
不能与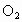 反应生成
反应生成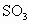
D.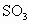 用98%的浓硫酸吸收,目的是防止形成酸雾,以使
用98%的浓硫酸吸收,目的是防止形成酸雾,以使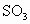 吸收完全
吸收完全
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能燃烧
B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com