
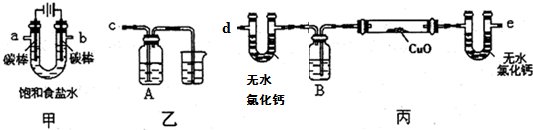
分析 (1)电解饱和氯化钠溶液时,阴极上氢离子放电,阳极上氯离子放电,同时生成氢氧化钠;用还原性物质检验氯气,用氧化铜检验氢气;
(2)①氯气有强氧化性,应该用强还原性的物质检验且反应现象明显,因为氯气有毒,所以不能直接排空,要有尾气处理装置;
②氢气在还原氧化铜之前要排尽装置内空气,否则会产生安全事故;
(3)根据质量差是否与铜有关来分析判断;利用差量法来计算铜的相对原子质量表达式;根据铜的相对原子质量的表达式确定影响高低.
解答 解:(1)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,溶液中同时生成氢氧根离子,所以电解反应离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,要检验氯气的氧化性,则氯气连接强还原性的物质且反应现象要明显,故选c,用氢气还原氧化铜来检验氢气,因为电解得到的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选e,
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;e;c;
(2)①氯气有毒,不能直接排空,氯气和水反应生成酸,所以氯气可以用碱性物质来处理,所以装置乙烧杯中液体的作用是吸收多余的氯气,防止环境污染;
氯气具有强氧化性,能氧化强还原性的物质,要检验氯气,必须选用强还原性的物质且反应现象明显,
a.氯气能氧化碘而使溶液褪色,氯气和水反应生成的次氯酸也能使溶液褪色,所以无法证明氯气的氧化性,故不选;
b.氯气和氢氧化钠溶液反应生成氯化钠和次氯酸钠,反应现象不明显,故不选;
c.氯气能把亚铁离子氧化成三价铁离子,铁离子和硫氰化钾溶液反应生成血红色溶液,反应现象明显,且能检验氯气的氧化性,故选;
d.氯气能氧化亚硫酸钠生成硫酸钠,但反应前后溶液颜色不变,反应现象不明显,故不选;
故答案为:吸收多余的氯气,防止环境污染;c;
②氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,加热氧化铜之前要通入氢气排尽装置内空气,故答案为:通入氢气排尽装置内空气;
(3)①中质量的差量是氢气还原氧化铜得到的物质,与铜有关,所以能计算铜的相对原子质量,②中质量的差量是氢气中原来的水蒸气,与铜无关,所以不能计算铜的相对原子质量,故选①;
硬质玻璃管中的质量差是氧元素的质量=m-m3,
设铜的相对原子质量为x,
CuO------O
1 16
$\frac{m}{x+16}$ m-m3
x=$\frac{16{m}_{3}}{m-{m}_{3}}$,
反应生成的铜被空气的氧气氧化使m3数据增大,则$\frac{16{m}_{3}}{m-{m}_{3}}$偏大,所以导致测定结果偏大,
故答案为:①;$\frac{16{m}_{3}}{m-{m}_{3}}$;偏大;反应生成的铜被空气的氧气氧化使m3数据增大,导致测定结果偏大.
点评 本题考查实验探究,难点是(3)题中确定影响铜的相对原子质量的大小,根据$\frac{16{m}_{3}}{m-{m}_{3}}$来分析即可,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | D的浓度减小了 | B. | A的转化率减小了 | ||
| C. | 物质B的质量分数增加了 | D. | a+b>c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时,v正(O2)=v逆(O2)=0必成立 | |
| B. | 关系式5v正(O2)=4v正(NO)总成立 | |
| C. | 在同一段时间范围内,用上述四种物质NH3、O2、NO、H2O的变化表示正反应速率的数值中,v正(H2O)最大 | |
| D. | 若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向装置中通入氮气且保持体积不变 | |
| B. | 向装置中通入稍过量氧气且保持体积不变 | |
| C. | 添加更多的催化剂 | |
| D. | 降低温度,及时转移SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用X表示此反应的反应速率是0.1amol•L-1•min-1 | |
| B. | 当混合气体的压强不再发生变化时,说明反应达到平衡状态 | |
| C. | 向平衡后的体系中加入1 mol M,平衡向逆反应方向移动 | |
| D. | 向上述平衡体系中再充入1 mol X,v正增大,v逆减小,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物 的名称为:2,6-二甲基-5-乙基庚烷 的名称为:2,6-二甲基-5-乙基庚烷 | |
| B. | 丙氨酸和苯丙氨酸脱水,最多可生成3种二肽 | |
| C. | 大气污染物氟利昂-12的化学式是CF2Cl2具有正四面体结构 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,甲比乙失电子多 | |
| B. | 同价态阳离子,甲比乙的氧化性强 | |
| C. | 甲能与冷水反应而乙不能 | |
| D. | 将甲、乙组成原电池时,乙为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用物质 A 表示的反应的平均速率为 0.3 mol•L-1•s-1 | |
| B. | 用物质 B 表示的反应的平均速率为 0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质 A 的转化率为70% | |
| D. | 2 s 时物质 B 的浓度为 0.7 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com