
 2Z(g)+W(g)�ﵽƽ��ʱ��VA=1.2aL��������˵��������ǣ�
2Z(g)+W(g)�ﵽƽ��ʱ��VA=1.2aL��������˵��������ǣ�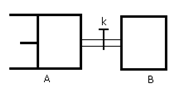
| A����Ӧ��ʼʱ��B�����л�ѧ��Ӧ���ʿ� |
| B��A������X��ת����Ϊ40%���ұ�B������X��ת���ʴ� |
| C����Kһ��ʱ���ƽ��ʱ��A�����Ϊ1.6aL����ͨ��������������ƣ� |
| D����K����ƽ�������B�����¶ȣ�A�������һ������ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ��Ũ��Ϊ0.6mol��L��1����ش��������⣺
��Ũ��Ϊ0.6mol��L��1����ش��������⣺ __________
__________ qC(g)���ܱ������н��С�
qC(g)���ܱ������н��С� ����.������������
����.������������
 Fe(SCN)3+3KCl��ƽ����ϵ�У��ش��������⣺
Fe(SCN)3+3KCl��ƽ����ϵ�У��ش��������⣺ ƽ�� _____________�ƶ���
ƽ�� _____________�ƶ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 I2(g)+H2(g)���ܱ������н��У��������е������е�ij���ʱ��仯ʱ������˵����Ӧ�ﵽƽ�����( )
I2(g)+H2(g)���ܱ������н��У��������е������е�ij���ʱ��仯ʱ������˵����Ӧ�ﵽƽ�����( )| A������ֵ����ʵ��� | B���������¶� | C��������ѹǿ | D������������ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ����ˮ��Һ�� | B��������������Һ�� |
| C������������������Ӧ�Ļ������ | D��ϡ�Ȼ���ˮ��Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��3.6��H | B��1.8��H |
| C��2��H | D��0.9��H |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
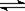 2SO3(g)��H����Q1 KJ/mol�����ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�����Q2KJ�����ϵʽ��ȷ����
2SO3(g)��H����Q1 KJ/mol�����ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�����Q2KJ�����ϵʽ��ȷ����| A��Q1��Q2 | B��Q1��Q2 | C��Q1��Q2 | D�����Ƚ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2(g)+3H2(g)
2(g)+3H2(g) 2NH3(g)�����ں��¡���ѹ��������ƽ��
2NH3(g)�����ں��¡���ѹ��������ƽ�� ��
�� ϵ��ͨ�������ƽ�� �ƶ�����������ҡ���������ʹ�ô��� ��Ӧ�ġ�H ���������С�����ı䡱����
ϵ��ͨ�������ƽ�� �ƶ�����������ҡ���������ʹ�ô��� ��Ӧ�ġ�H ���������С�����ı䡱�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
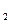 �����2.0 mol SO
�����2.0 mol SO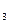 �������ڹ̶�������ܱ������У���һ�������·�����Ӧ��2SO2(g)+O2(g)
�������ڹ̶�������ܱ������У���һ�������·�����Ӧ��2SO2(g)+O2(g) 2
2 SO3(g)���ﵽƽ��ʱSO3Ϊn mol ������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol���� �� ��
SO3(g)���ﵽƽ��ʱSO3Ϊn mol ������ͬ�¶��£��ֱ������������ͬ�ܱ������з�����ʼ���ʣ�ƽ��ʱSO3����n mol���� �� ��| A��1.6 mol SO2+0.3 mol O2+0.4 mol SO3 | B��3.0 mol SO2+1.0 mol O2+1.0 mol SO3 |
| C��2.0 mol SO2+1.0 mol O2+2.0 mol SO3 | D��4.0 mol SO2+1.0 mol O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 cC��g����
cC��g����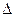 H��0���ڵ��������½��С��ı�������Ӧ��������I��II��III����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
H��0���ڵ��������½��С��ı�������Ӧ��������I��II��III����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
 ��
��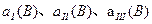 ����С���� ����ֵ�� ��
����С���� ����ֵ�� ��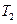 ���͵�III�η�Ӧ�ٶȣ�
���͵�III�η�Ӧ�ٶȣ�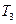 ���ĸߵͣ�
���ĸߵͣ�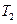
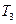 ��������������жϵ������� ��
��������������жϵ������� ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com