
| A、OH-+CO32-+2H+→HCO3-+H2O |
| B、2OH-+CO32-+3H+→HCO3-+2H2O |
| C、2OH-+CO32-+4H+→CO2↑+3H2O |
| D、OH-+CO32-+3H+→CO2↑+2H2O |


科目:高中化学 来源: 题型:
A、CaCO3
| ||||
B、CuO+CO
| ||||
| C、NaOH+HCl═H2O+NaCl | ||||
| D、CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8种;2种 |
| B、8种;3种 |
| C、7种;3种 |
| D、7种;2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构 |
| B、sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |
| C、分子间氢键会使物质的熔点沸点升高,而分子内氢键对熔沸点影响不大 |
| D、杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、新药帕拉米韦对禽流感H7N9有显著疗效,它的结构简式为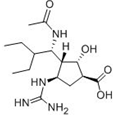 化学式是C15H26N4O4 化学式是C15H26N4O4 |
| B、2013年11月20日山东现‘夺命快递’----化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯它是无色透明液体,溶于乙醇、乙醚,不溶于水.它属于酯类,也属于卤代烃 |
C、绿原酸的结构简式为: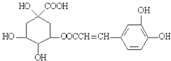 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 |
D、苯的同系物 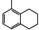 ,其所有碳原子不可能在同一平面上 ,其所有碳原子不可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
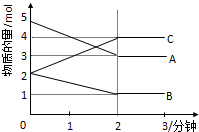 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示:
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
| 时间(min) | 20 | 25 | 30 | 40 | 50 | 60 |
| CH2(OCH3)2(mol/L) | 9.02 | 9.10 | 9.18 | 9.23 | 9.30 | 9.32 |
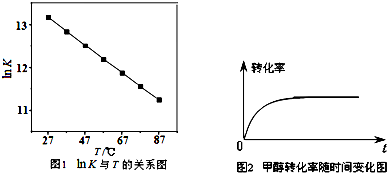
| 影响因素 试验号 |
甲醛的滴加速率(g/min) | 反应时间(min) | 催化剂的量(g) | 搅拌速率 |
| 1 | 70 | 2.5 | 30 | |
| 2 | 1.0 | |||
| 3 | 2.5 | 80 |
| CH3OH |
| H+ |
| CH3OH |
| -H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题:
如图所示的两个实验装置中,均为500mL氯化铜溶液,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com