
【题目】在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是

A.t时,X、Y、Z的质量不再改变
B.该反应的化学方程式为:3Z=3X+2Y
C.t时,Z的浓度为1.2mol/L
D.t时,反应停止,反应速率为0
【答案】A
【解析】
根据图象,Z的物质的量逐渐减少,X、Y的物质的量逐渐增大,说明Z为反应物,X、Y为生成物,最终达到平衡状态,说明为可逆反应,结合物质的量的变化关系判断反应的方程式,再结合化学反应速率和平衡状态的特征分析判断。
A.根据图象,t时为平衡状态,化学平衡时各组分的浓度不再随时间变化而变化,故X、Y、Z的质量也不再改变,故A正确;
B.由图可知,X、Y的物质的量增大,为生成物,Z物质的量减小,为反应物,到达平衡后,X生成1.8mol,Y生成1.2mol,Z反应1.8mol,X、Y、Z的化学计量数之比=1.8∶1.2∶1.8=3∶2∶3,则反应的化学方程式为:3Z3X+2Y,故B错误;
C.根据图象可知,平衡时Z的浓度为![]() =0.6mol/L,故C错误;
=0.6mol/L,故C错误;
D.t时为平衡状态,反应处于平衡时正、逆反应速率相等,但不等于零,故D错误;
故选A。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】甲醇是重要的绿色能源之一,目前科学家用水煤气(CO+H2)合成甲醇,其反应为:CO(g)+2H2(g) ![]() CH3OH(g)△H=-128.1kJ·mol-1
CH3OH(g)△H=-128.1kJ·mol-1
回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有_____。
A、升高温度 B、增大压强 C、充入氢气 D、分离出甲醇
(2)恒温恒容条件能说明该可逆反应达平衡的是_________;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中充入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。
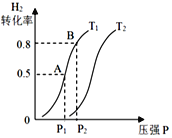
①该反应的△S____0,图中的T1___T2(填“<”“>”或“=”)
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为______,若达到平衡状态B时,则容器的体积V(B)=______L。
(4) CO燃烧的热化学方程式:CO(g)+ 1/2 O2(g)═CO2(g)△H= —283.0kJmol-1
H2(g)+1/2 O2(g)═H2O(l)△H= —285.8 kJmol-1
CO(g)+2H2(g)═CH3OH(l)△H= —128.1KJmol-1
则CH3OH(g)燃烧热的热化学方程式是为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在医药卫生、高纯度金属提炼、光学仪器等领域起着至关重要的作用。从含碘化钾废液(可能还含有I2、IO3-)中回收I2,实验过程如下:
(1)确定碘的存在形式
①I2的确定:取含碘废液放入试管,加入CCl4,振荡静置,现象为_____,确定含有I2。
②IO3-的确定:取①中上层溶液,加入少量新配制的0.1mo/LFeSO4溶液,它的作用是____。振荡使之充分反应,再加入少量CCl4,CCl4层无紫色出现,说明该含碘废液中无IO3-。
(2)碘的回收
在含碘废液中加入适量的K2Cr2O7溶液和稀H2SO4,充分反应后经减压过滤得到粗碘,由粗碘提纯精制碘的装置如图:
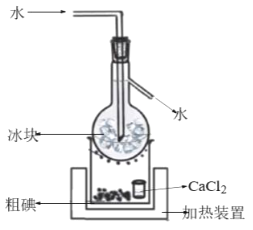
①补全得到粗碘的离子方程式:______。
□Cr2O72-+□I-+□ =□ +□Cr3++□ 。
②CaCl2的作用是__。
(3)碘的纯度分析(已知:2S2O32-+I2=2I-+S4O62-)
精确量取0.1136g精制后的碘置于250mL碘量瓶中,加入0.5gKI和30mL水,振荡至完全溶解(KI仅用于溶解)。以0.0513mol·L-1的Na2S2O3溶液快速滴定至淡黄色,加入1mL左右淀粉溶液,缓慢滴定至____,消耗Na2S2O3溶液17.26mL。碘的纯度的计算表达式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3═2A+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为________,含有的化学键类型为_________________。
(2)生成物中含有一个10个电子的分子,该分子的空间构型为________,中心原子的杂化方式为________。
(3)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是________(填微粒符号)。
(4)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。则一个晶胞中Al原子的数目为________个。
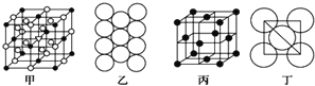
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )

A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液不显色
C. 1 mol该物质与溴水反应,最多消耗2 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对应的离子方程式正确的是( )
A.铝溶解在NaOH溶液中:2Al+2OH-=2AlO2-+3H2↑
B.向溴水中通入SO2后褪色:SO2+Br2+2H2O=SO42-+2Br-+4H+
C.白醋与84消毒液混合产生黄绿色气体:Cl-+ClO-+2H+=Cl2↑+H2O
D.少量铁溶于过量稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是化学反应中的能量变化图,该反应方程式为A2+B2==2AB,回答下列问题

(1)该反应中,反应物断键吸收的能量为_______________kJ/mol,生成物成键释放的能量为_______________kJ/mol属于_______________(填“放热”“吸热”)反应,该反应的该反应的△H=_______________(用字母写出表达式)
(2)已知反应有下列反应
①Fe+2HCl=FeCl2+H2↑ ②H2SO4+2NaOH=Na2SO4+2H2O
③CO+CuO=Cu+CO2↑ ④Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
与图片所示化学反应热效应相同的是_______________(填序号)
(3)以下说法正确的是_______________
A.中和反应是吸热反应
B.铝热反应需要在高温条件下进行,铝热反应属于吸热反应
C.放热反应发生时有可能需要加热
D.凡是放出热量的化学反应均可用来造福人类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,完全正确的一组是
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过![]() 容积的试管加热
容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤加热坩埚要垫上石棉网
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧将滴管竖直伸入试管内滴加液体
⑨稀释浓硫酸时,应沿器壁缓缓地将水加入浓硫酸中
⑩用镊子从煤油中取出金属钠,再用小刀切一小块,然后将剩下的钠放回原瓶
A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最早的麻醉药是从南美洲生长的古柯植物提取的可卡因,目前人们已实验并合成了数百种局部麻醉剂,多为羧酸酯类。F是一种局部麻醉剂,其合成路线:
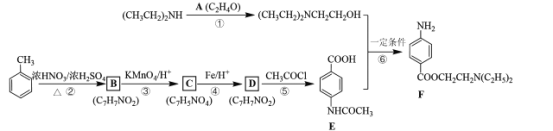
回答下列问题:
(1)已知A的核磁共振氢谱只有一个吸收峰,写出A的结构简式____。
(2)B的化学名称为________。
(3)D中的官能团名称为____,④和⑤的反应类型分别为________、____。
(4)写出⑥的化学方程式____。
(5)C的同分异构体有多种,其中-NO2直接连在苯环上且能发生银镜反应的有_____种,写出其中苯环上一氯代物有两种的同分异构体的结构简式____________。
(6)参照上述流程,设计以对硝基苯酚钠、乙醇和乙酰氯(CH3COCl)为原料合成解热镇痛药非那西丁(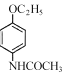 )的合成路线(无机试剂任选)。已知:
)的合成路线(无机试剂任选)。已知: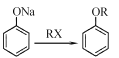 __________
__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com