
【题目】Ⅰ掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为三套实验装置。

(1)写出下列仪器的名称:a.__________,b._____________。
(2)若利用装置1分离四氯化碳和酒精的混合物,还缺少的仪器是__________,将仪器补充完整后进行实验,冷凝水由________(填f或g) 口通入。
(3)用装置II分离混合物时,为使液体顺利流下,应进行的操作是_______________。
(4)实验室用Na2CO3·10H2O 晶体配制0.05mol/L 的Na2CO3 溶液970mL。
①应用托盘天平称取Na2CO3·10H2O 的质量是____g。
②装置III是某同学转移溶液的示意图。图中的错误是_______________。
③除了图中给出的仪器和托盘天平以及烧杯外,为完成实验还需要的仪器有:______________。
Ⅱ利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
(1)溶液配制:称取1.200 0 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在________中溶解,完全溶解后,全部转移至100 mL的________中,加蒸馏水至________。
(2)滴定:取0.00950 mol·L-1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:Cr2O72-+6I-+14H+===3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-===S4O62-+2I-。加入淀粉溶液作为指示剂,继续滴定,当溶液______,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为______%(保留1位小数)。
【答案】蒸馏烧瓶 冷凝管 酒精灯 g 打开分液漏斗上口的玻璃塞 143 未用玻璃棒引流 药匙、量筒、玻璃棒、胶头滴管 烧杯 容量瓶 凹液面最低处与刻度线相平 由蓝色变为淡黄绿色且半分钟不变化 95.0
【解析】
Ⅰ(1)由图及仪器的结构可知仪器的名称;
(2)冷却水在冷凝管中下进上出;
(3)为使液体顺利流下,需先打开分液漏斗上口的玻璃塞;
(4)①配制0.05mol/L 的Na2CO3 溶液970mL,应选用1000ml的容量瓶;
②转移溶液应用玻璃棒引流;
③根据配制溶液的实验操作过程选择所用仪器;
Ⅱ(1)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作;
(2)根据方程式中 I2、S2O32-之间的关系式计算。
Ⅰ(1)由图可知,a为蒸馏烧瓶,b为冷凝管;
(2)若利用装置1分离四氯化碳和酒精的混合物,进行的实验操作的名称为蒸馏,需要加热,故还缺少的仪器有酒精灯,实际操作时冷却水在冷凝管中下进上出,冷凝水由g口通入;
(3)装置II可用于分液,分离互不相溶的液体混合物,为使液体顺利流下,需要平衡内外压强,故应进行的操作是:打开分液漏斗上口的玻璃塞;
(4)Na2CO3·10H2O 的质量=1L×0.05mol/L×286g/mol=14.3g;
②转移溶液应用玻璃棒引流,防止溶液外溅,造成浓度偏低;
③操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解。冷却后转移到1000mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀。所用仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、1000mL容量瓶、胶头滴管。根据提供仪器,所以还需仪器有药匙、量筒、玻璃棒、胶头滴管;
Ⅱ(1)溶液配制:称取1.200 0 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在烧杯中溶解,完全溶解后,冷却至室温后,全部转移至100 mL的容量瓶中,将洗涤液转移至容量瓶,振荡后加蒸馏水至凹液面最低处与刻度线相平;
(2)加入淀粉溶液作为指示剂,继续滴定,当溶液由蓝色变为淡黄绿色且半分钟不变化,即为终点。根据方程式,Cr2O72-~3I2~6S2O32-,得n(Na2S2O35H2O)=n(S2O32-)=0.00950 mol·L-1×0.02L×6=1.14×10-3mol,样品中m(Na2S2O35H2O)=1.14×10-3mol×248 g/mol×![]() =1.14g,质量分数=
=1.14g,质量分数=![]() ×100%=95%。
×100%=95%。


科目:高中化学 来源: 题型:
【题目】有机物AH的转化关系如下图所示。其中A是植物生长调节剂,它的产量可以用来衡量一个国家的石油化工发展水平;D是一种合成高分子材料,此类物质如果大量使用易造成“白色污染”。

请回答下列问题:
(1)E官能团的电子式为_____。
(2)关于有机物A、B、C、D的下列说法,不正确的是____(选填序号)。
a. A、B、C、D均属于烃类
b. B的同系物中,当碳原子数≥4时开始出现同分异构现象
c. 等质量的A和D完全燃烧时消耗O2的量相等,生成CO2的量也相等
d. B不能使溴水或酸性高锰酸钾溶液褪色,但A和D可以
(3)写出下列反应的化学方程式:
反应③:____________________________;
反应⑥:_____________________________。
(4)C是一种速效局部冷冻麻醉剂,可由反应①或②制备,请指出用哪一个反应制备较好:_______,并说明理由:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双极电化学法(装置如图)是在传统电解装置中放置了导电性电极BPE,通电时,BPE两端界面产生电势差,生成梯度合金。下列有关说法错误的是

A.m为电源负极
B.BPE的b端比a端的电势高
C.BPE的a端发生的反应为: 2H2O+2e-=H2↑+2OH-
D.BPE的b端到中心的不同位置,能形成组成不同的铜镍合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空题
(1)“金属钙线”是炼制优质钢材的脱氧脱磷剂,某“金属钙线”的主要成分为金属M和金属钙Ca,并含有3.5%(质量分数)CaO.
①Ca元素原子结构示意图________,Ca(OH)2碱性比Mg(OH)2______(填“强”或“弱”).
②配平用“金属钙线”脱氧脱磷的方程式:___P +____FeO +____CaO![]() ____Ca3(PO4)2 +____Fe
____Ca3(PO4)2 +____Fe
③将“金属钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色的M(OH)n,该颜色变化过程的化学方程式为:_____________________,实验室检测Mn+最常用的试剂是___________(填化学式)
④取3.2 g“金属钙线”试样,与水充分反应,生成448 mL H2(标准状况),在所得溶液中通入适量的CO2,最多能得到CaCO3________g,“金属钙线”试样中金属M的质量分数为______.
(2)氢化钙(CaH2)固体登山运动员常用的能源提供剂
①写出CaH2与水反应的化学方程式__________________,该反应的氧化产物是___.
②请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象_____.
③登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ(1)标准状况下,1.7 g NH3与_______L H2S气体含有的氢原子数相同。
(2)2 mol的CO2与3 mol的SO3的原子数之比是__________。
(3)常温常压下22.4升CO2中分子个数___64克SO2的分子个数(填“>、<或=”)
(4)标准状况下,33.6L的NH3所含电子的物质的量约为______mol,将其溶解于水配成1L的溶液,则溶液的物质的量浓度为__________mol/L
(5)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积为________。
(6)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣,测得Na+、Mg2+ 和Cl﹣的物质的量浓度依次为:0.2molL﹣1、0.25molL﹣1、0.4molL﹣1,则c(SO42﹣)=__________.
(7)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为_____________。
(8)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L,该混合气体的平均摩尔质量为_________________,NH3的体积分数为______________.
(9)VmLAl2(SO4)3溶液中含Al3+ ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度是_____________mol/L。
Ⅱ.请按照要求完成下列方程式。
(1)写出泡沫灭火器反应原理的离子方程式:_______________________________________。
(2)铁与水蒸气高温下反应的化学方程式:____________________________________________。
(3)NaCN属于剧毒物质,有一种处理方法其原理为CN-与S2O32-反应生成两种离子,一种与Fe3+可生成红色溶液,另一种与H+作用产生能使品红溶液褪色的刺激性气体,写出CN-与S2O32-反应的离子方程式:___________________________________。
(4)亚硝酸盐是毒性较强的物质,其具有较强的还原性,将亚硝酸钠溶液滴加到K2Cr2O7酸性溶液(橙色)中,溶液由橙色变为绿色(Cr3+),试写出反应的离子方程式:__________________________。
(5)将NaHSO4溶液滴入氢氧化钡溶液中至中性的离子反应方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其化合物在工业生产生活中有很重要的作用。已知:实验室中可用KClO3与浓盐酸发生如下反应:
(_____)KClO 3+(_____)HCl(浓)-(_____)KCl+(_____)Cl2↑+(____) H2O,
(1)请配平该反应,并用双线桥法标出电子转移的方向和数目。______________
(2)该反应中氧化剂为______;氧化剂与还原剂的物质的量之比为______;氧化产物与还原产物的物质的量之比为______;被氧化的元素和被还原的元素的质量之比为_________。
(3)浓盐酸在反应中表现出来的性质是________________(填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸
(4)当此反应中产生标准状况下13.44L的Cl2 ,则该反应转移的电子的数目为_____;被氧化的盐酸的物质的量为______mol,参加反应的盐酸的物质的量为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:
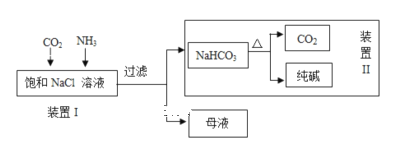
(1)工业生产纯碱的第一步是除去饱和食盐水的中SO42-、Ca2+离子,依次加入的试剂及其用量是______________、_______________、过滤、_______________。
(2)已知:几种盐的溶解度
NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
①写出装置I中反应的化学方程式_____________________________________。
②写出装置II中发生反应的化学方程式________________________________。
(3)该流程中可循环利用的物质是__________________。
(4)若制出的纯碱中只含有杂质NaCl。
①检验用该纯碱配制的溶液中含有Cl―的方法是_________________________。
②向m克纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g,则该纯碱的纯度(质量分数)为__________(用m、b来表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中I、II两个反应属于同一反应类型的是( )
选项 | 反应I | 反应II |
A |
| CH2=CH2→CH3CH2Cl |
B | CH3CH2Cl→CH3CH2OH | CH3CH2OH→CH3COOCH2CH3 |
C | CH3CH2OH→CH2=CH2 | CH3CH2OH→CH3CHO |
D | 油脂→甘油 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,有四种气体:①6.72 L CH4;②3.01×1023个HCl分子;③13.6g H2S;④0.2 mol NH3。下列有关比较中正确的是
A.体积大小:②>③>①>④
B.质量大小:②>③>④>①
C.氢原子数目多少:④>①>③>②
D.摩尔质量的大小:④>②>③>①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com