
【题目】杂志Joule中题为“Li—CO2 Electrochemistry:A New Strategy for CO2 Fixation and Energy Storage”的文章,阐述关于电化学技术固定CO2新的反应途径。下图是采用新能源储能器件将CO2转化为固体产物,实现CO2的固定和储能灵活应用的装置。储能器件使用的Li—CO2电池组成为钌电极/CO2—饱和LiClO4—DMSO电解液/锂片。下列说法错误的是
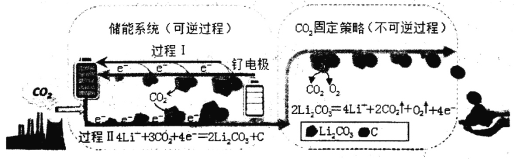
A.钌电极为负极,其电极反应式为:2Li2CO3+C—4e-=== 3CO2+4Li+
B.Li—CO2电池电解液由LiClO4—DMSO溶于水得到
C.这种电化学转化方式不仅减少CO2的排放,还可将CO2作为可再生能源载体
D.CO2的固定中,每生成1.5mol气体,可转移2mole-
【答案】B
【解析】
A.由图可知,钌电极上的电极反应式为 2Li2CO3+C-4e-=4Li++3CO2↑,故A正确;
B. 由题意可知,Li-CO2 电池有活泼金属 Li,所以电解液为非水溶液饱和LiClO4-(CH3)2SO(二甲基亚砜)有机溶剂,故B错误;
C. 由图可知,CO2通过储能系统和CO2固定策略转化为固体产物C,这种电化学转化方式不仅减少CO2的排放,还可将CO2作为可再生能源载体,故C正确;
D. 由图可知,CO2的固定中的电极反应式为:2Li2CO3=4Li++2CO2↑+O2+4e-,转移4mole-生成3mol气体,CO2的固定中,每生成1.5mol气体,可转移2mole-,故D正确;
故选B。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O
B. 酸性高锰酸钾溶液与稀草酸反应:5C2O42-+2MnO4-+16H+===2Mn2++10CO2+8H2O
C. AgCl的悬浊液中滴加Na2S溶液:2AgCl+S2-===Ag2S+2Cl-
D. NH4HCO3溶液加入过量NaOH溶液加热:NH4++OH-===NH3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作及现象结论描述不准确的是( )
A.向沸水中滴加饱和氯化铁溶液制备胶体,用可见光束照射,产生丁达尔效应
B.常温下,向0.10mol·L-1 NaHCO3溶液,滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出,说明加入CaCl2促进了HCO3-的水解
C.利用以下实验器材(规格数量不限):烧杯、量筒、环形玻璃搅拌棒、纸条、硬纸板、温度计能完成中和反应反应热的测定
D.向浓度均为0.1mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,先出现蓝色沉淀,因为KSP[Mg(OH)2]>KSP[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
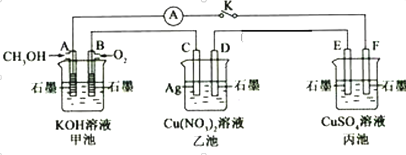
(1)甲池为__________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为______________。
(2)丙池中E电极为_________(填“正极”、“负极”、“阴极”或“阳极”),电极的电极反应式为_____________。该池总反应的化学方程式为___________________。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_____mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关图所示原电池的叙述正确的是
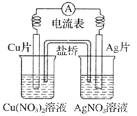
A.电流沿导线由Cu片流向Ag片
B.正极的电极反应是Ag++e-=Ag
C.Cu片上发生还原反应,Ag片上发生氧化反应
D.反应时盐桥中的阳离子移向Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,某科研小组设计如下工艺流程回收铜并制取胆矾(流程中RH为萃取剂),下列说法正确的是

A.反应I的离子方程式为:Cu+H2O+2NH3+2NH4+==Cu(NH3)42++2H2O
B.操作②用到的主要仪器为蒸馏烧瓶
C.操作④以石墨为电极电解硫酸铜溶液:阳极产物为O2和H2SO4
D.操作⑤为:蒸发浓缩、冷却结晶、过滤、热水洗涤、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法错误的
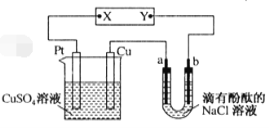
A.X极是电源正极,Y极是电源负极B.Cu电极上增重6.4g时,b极产生2.24 L气体
C.电解过程中CuSO4溶液的pH逐渐减小D.a极的电极反应式为2Cl――2e-=Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
反应1:Fe2O3(s)+3C(石墨,s) ![]() 2Fe(s)+3CO(g) △H 1
2Fe(s)+3CO(g) △H 1
反应2:C(石墨,s)+CO2(g)![]() 2CO(g) △H 2
2CO(g) △H 2
①△H=__(用含△H1、△H2代数式表示)
②保持温度不变,在恒容容器中进行反应1,达到平衡状态,再次充入一定量的CO(Fe足量),则平衡__移动(填“正向”或“逆向”),达到新平衡后c(CO)将__(填“变大”、“变小”或“不变”)
(2)氯化铵常用作除锈剂,其水溶液呈酸性的原因是__。
(3)硫酸铝水解的离子方程式是__,为了抑制其水解,配制时可以加入少量的__。
(4)泡沫灭火器中装的灭火剂主要包括硫酸铝溶液、碳酸氢钠溶液。泡沫灭火器内置的玻璃筒应装__溶液,外部的铁筒装另一种溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 m、n、p、q 在元素周期表中的排列如图所示,其中 n 的最高价氧化对应的水化物既能与强酸反应,也能与强碱反应,下列说法正确的是( )
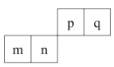
A.元素n位于元素周期表第3周期,第ⅢA族
B.单质与水反应置换出氢气的能力:m<n
C.简单离子半径:m>q
D.最高价氧化物对应水化物的碱性:m<n
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com