
| A、用干冰保藏易变质的食品 |
| B、用硫磺熏制白木耳、粉丝等食品 |
| C、用甲醛浸泡易腐烂的食品 |
| D、用含亚硝酸钠的工业用盐腌制食品 |


科目:高中化学 来源: 题型:
| A、①=③>② |
| B、③>②>① |
| C、③=②>① |
| D、①=②=③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
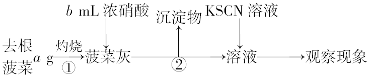
| O | 2- 3 |
| O | 2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶中含有少量蒸馏水 |
| B、将溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
| C、定容时观察液面俯视 |
| D、定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)>c(OH-) |
| B、c(HCN)>c(CN-) |
| C、c(HCN)>c(CN-)=0.2 mol?L-1 |
| D、c(CN-)>c(OH-)=0.1 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
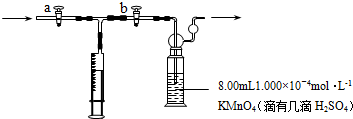
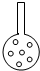
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com