
| A. | X是最简单的芳香烃,分子中含有三个碳碳双键 | |
| B. | Y是具有芳香气味的液体,难溶于水,易溶于有机溶剂,能发生水解反应 | |
| C. | Z是无色,有特殊香味的液体,与硫酸混合在140℃可以制备乙烯 | |
| D. | W是有强烈刺激性气味的无色液体,可与氢气发生加成反应,生成Z |
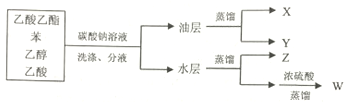
分析 乙酸和乙醇易溶于饱和碳酸钠溶液,而乙酸乙酯、苯不易溶于饱和碳酸钠溶液,所以向混合物中加入碳酸钠溶液洗涤、分液后得到的油层含有乙酸乙酯和苯、水层含有乙醇和乙酸钠、碳酸钠,油层蒸馏得到X和Y,X不能与NaOH溶液反应,则X是苯、Y为乙酸乙酯;
水层蒸馏得到Z为乙醇,用浓硫酸蒸馏得到的W为乙酸,
A.X是苯,苯中不含碳碳双键;
B.Y是乙酸乙酯,含有酯基的物质难溶于水,易溶于有机溶剂,能发生水解反应;
C.Z是乙醇,能在浓硫酸作催化剂、加热170℃条件下发生消去反应;
D.W是乙酸,羧基不能发生加成反应.
解答 解:乙酸和乙醇易溶于饱和碳酸钠溶液,而乙酸乙酯、苯不易溶于饱和碳酸钠溶液,所以向混合物中加入碳酸钠溶液洗涤、分液后得到的油层含有乙酸乙酯和苯、水层含有乙醇和乙酸钠、碳酸钠,油层蒸馏得到X和Y,X不能与NaOH溶液反应,则X是苯、Y为乙酸乙酯;
水层蒸馏得到Z为乙醇,用浓硫酸蒸馏得到的W为乙酸,
A.X是苯,苯中不含碳碳双键,苯中碳碳之间的化学键是介于单键和双键之间的特殊键,故A错误;
B.Y是乙酸乙酯,含有酯基的物质难溶于水,易溶于有机溶剂,能发生水解反应,乙酸乙酯含有酯基,所以难溶于水,易溶于有机溶剂,具有香味,酸性或碱性条件下能发生水解反应生成羧酸或酸式盐和乙醇,故B正确;
C.Z是乙醇,能在浓硫酸作催化剂、加热170℃条件下发生消去反应生成乙烯,乙醇是无色有特殊香味的液体,故C错误;
D.W是乙酸,羧基不能发生加成反应,所以乙酸不能和氢气发生加成反应,故D错误;
故选B.
点评 本题考查有机物分离和提纯,为高频考点,明确常见有机物官能团及其性质关系、常见反应类型、反应条件是解本题关键,会利用物质性质差异性分离提纯,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 在蒸发皿中灼烧CuSO4•5H2O晶体以除去结晶水 | |
| B. | 配制0.1 mol•L-1硫酸溶液时,容量瓶应先用0.1 mol•L-1硫酸溶液润洗 | |
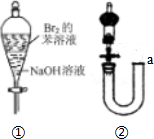
| C. | 用图①所示装置实验,振荡后静置,溶液不再分层,且保持无色透明 | |
| D. | 沿图②中的a口加水,可以检验该装置的气密性. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
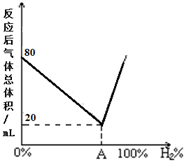 ①某烷烃分子式为C6H14,若该烷烃可由两种炔烃与氢气加成得到,则该烷烃的结构简式为(CH3)2CHCH2CH2CH3.
①某烷烃分子式为C6H14,若该烷烃可由两种炔烃与氢气加成得到,则该烷烃的结构简式为(CH3)2CHCH2CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
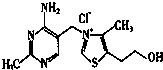
| A. | 分子中四个原子共直线,且C为SP杂化 | |
| B. | 分子中N≡C键的键长大于C-C键的键长 | |
| C. | 分子中含有2个σ键和4个π键 | |
| D. | 不和氢氧化钠溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C16H16O9 | |
| B. | 能与碳酸钠溶液反应,但不产生二氧化碳 | |
| C. | 能发生催化氧化反应并生成能发生银镜反应的产物 | |
| D. | NaOH、H2、溴水分别与1mol绿原酸反应时,消耗反应物的最大物质的量都为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60 g SiO2晶体中含有2×6.02×1023个Si-O键 | |
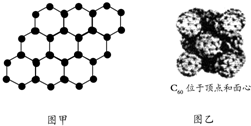
| B. | 石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如图甲),则0.12 g石墨烯中含有6.02×1022个碳原子 | |
| C. | 720 g C60晶体(如图乙)中含有6.02×1023个晶胞结构单元 | |
| D. | 14 g两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目为3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
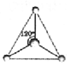 CH3+;
CH3+;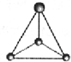 CH3-.
CH3-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com