
| A. | 碱金属的密度随着原子序数的递增逐渐减小 | |
| B. | 钾与氧气或水反应比钠与氧气或水反应剧烈,铷、铯的相应反应更剧烈 | |
| C. | 随着原子序数的递增碱金属单质的熔沸点升高 | |
| D. | 碱金属元素阳离子的氧化性随着原子序数的递增依次增强 |
分析 A.碱金属的密度随着原子序数的递增逐渐减小(但是K反常);
B.第ⅠA族元素单质的活泼性逐渐增强;
C.随着原子序数的递增碱金属单质的熔沸点降低;
D.碱金属元素从上到下阳离子的氧化性逐渐减弱.
解答 解:A.碱金属的密度随着原子序数的递增逐渐减小,但是K反常,故A错误;
B.第ⅠA族元素单质的活泼性逐渐增强,所以钾与氧气或水反应比钠的反应剧烈,铷、铯的反应更剧烈,故B正确;
C.随着原子序数的递增,碱金属的原子半径增大,金属键减弱,所以碱金属单质的熔沸点降低,故C错误;
D.碱金属元素从上到下随着原子序数的递增,单质的还原性逐渐增强,阳离子的氧化性逐渐减弱,故D错误.
故选:B.
点评 本题考查碱金属的性质,把握碱金属性质的递变规律为解答的关键,注意原子结构决定性质,明确元素周期律的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属钠、碳化钙着火时,可直接用高压水枪喷火扑灭 | |
| B. | 去除银器表面的Ag2S,可将银器放在盛有食醋的铝锅中煮沸 | |
| C. | 苹果在空气中久置变黄和纸张变黄的原理相似 | |
| D. | 用乙醚从黄花蒿中萃取青蒿素发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
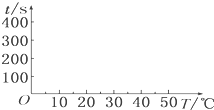 在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:| 编号 | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶解 的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 细小颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
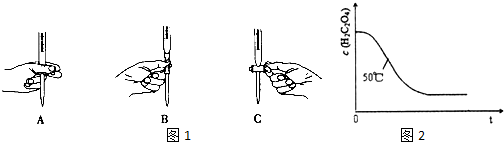
| 实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2探究探究温度不同对反应速率的影响; b.实验1和3探究反应物浓度对该反应速率的影响; c.实验1和4探究催化剂对该反应速率的影响. | |
| 体积 (mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1次 | 第2次 | 第3次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3过量 | |
| B. | AlCl3的量恰好与氢氧化钠完全反应 | |
| C. | 两种碱均过量 | |
| D. | AlCl3的量恰好与氨水完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b-a-4 | B. | b-a-8 | C. | b+a+8 | D. | b-a-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com