
锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O=2Zn(OH)42-。下列说法正确的是
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-)逐渐减小
C.放电时,负极反应为:Zn+4OH–-2e–=Zn(OH)42-
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2017届贵州省高三上联考四化学试卷(解析版) 题型:选择题
短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的焰色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z的核电荷数是W的2倍,Y是地壳中含量最多的金属元素。下列说法不正确的是
A. 工业上常用电解的方法制备X、Y的单质
B. 元素Q和Z能形成QZ2型的共价化合物
C. 原子半径的大小顺序:r(X)>r(Y)>r(W)>r(Q)
D. 元素X、Y、Z的最高价氧化物对应的水化物之间能相互发生反应
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上月考三化学试卷(解析版) 题型:填空题
重铬酸钾是一种常见的强氧化剂。实验室以精选铬铁矿(主要成分可表示FeO·Cr2O3,还含有 SiO2、 Al2O3 等杂质)为原料制备重铬酸钾晶体(K2Cr2O7,式量294)的流程如下:
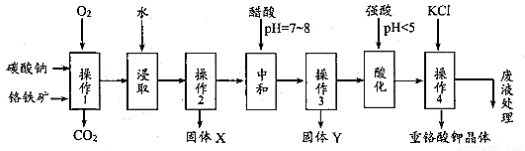
请回答下列问题:
操作1中发生的反应有:
4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
Na2CO3+Al2O3 2NaAlO2+CO2↑;Na2CO3+SiO2
2NaAlO2+CO2↑;Na2CO3+SiO2 Na2SiO3+CO2↑
Na2SiO3+CO2↑
该步骤在常温下的反应速度较慢,为使反应速率增大,可采取的两条措施是____________。
(2)固体Y 中主要含有______________。(填写化学式)
(3)酸化步骤使含铬物质发生了转化,请写出离子反应方程式______________________。
(4)操作 4 中的化学反应在溶液中能发生的可能理由是_________________________;获得 K2Cr2O7 晶体的操作依次是:加入KCl 固体,在水浴上加热浓缩至______________,冷却结晶,抽滤,洗涤,干燥。
(5)通过下列实验可测定产品中重铬酸钾的质量分数:称取重铬酸钾试样 1.470g,用100mL 容量瓶配制成溶液。移取25.00mL 溶液于碘量瓶中,加入适里稀硫酸和足量碘化钾(铬的还原产物为 Cr3+),放于暗处 5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/L 标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:I2+2S2O32-=2I-+S4O62-;则所测产品中重铬酸钾的纯度为_____________。
(6)有关上述实验过程中涉及的部分实验操作的描述,正确的是_________.
A.粗产品若要进一步提纯,可以采用重结晶的方法
B. 配制溶液时,用托盘天平称取试样后,一般经溶解、转移(含洗涤)、定容等步骤,配制成100mL溶液
C.滴定时,当最后一滴标准溶液滴入时,溶液变为蓝色,且半分钟内不变色,可判断滴定终点
D.滴定终点时俯视读数,测定结果偏低
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考五化学试卷(解析版) 题型:选择题
某电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。该电池是以K2FeO4和Zn为电极材料,KOH溶液为电解 溶质溶液,其总反应为:3Zn+2K2FeO4+8H2O
溶质溶液,其总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列说法正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列说法正确的是
A.Zn为电池的正极
B.充电时阳极反应为:Fe(OH)3-3e?+5OH? =FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.该电池放电过程中电解质溶液浓度不变
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考二化学卷(解析版) 题型:实验题
CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s)+3HCl(aq)  H3CuCl4(aq)。
H3CuCl4(aq)。
(1)实验室用下图所示装置制取CuCl,反应原理为:
2Cu2++SO2+8Cl-+2H2O=2CuCl43-+SO42-+4H+
CuCl43-(aq) CuCl(s)+3Cl-(aq)
CuCl(s)+3Cl-(aq)
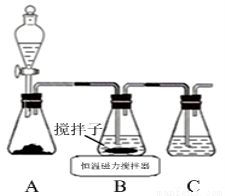
①装置C的作用是 。
②装置B中反应结束后,取出混合物进行如下图所示操作,得到CuCl晶体。

操作ⅱ的主要目的是 ;操作ⅳ中宜选用的试剂是 。
③实验室保存新制CuCl晶体的方法是 。
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案: 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成。
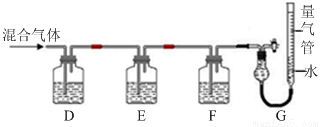
已知:i.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O。
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
D、F洗气瓶中宜盛放的试剂分别是 、 。
②写出保险粉和KOH的混合溶液吸收O2的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考二化学卷(解析版) 题型:选择题
用下图所示实验装置进行相应实验,能达到实验目的的是

A.用图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体
B.按装置②所示的气流方向可用于收集H2、NH3等
C.用图④所示装置,分离CCl4萃取I2水后的有机层和水层
D.用图④所示装置,可以证明氧化性Cl2>Br2>I2
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上适应性训练四化学卷(解析版) 题型:实验题
【化学—选修5:有机化学基础】
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
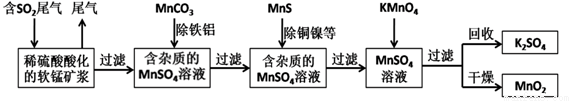
请回答下列问题:
(1)上述流程中多次设计到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、烧杯,_______________;其中玻璃棒的作用是___________________。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是_____________(只用文字表述)
(3)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中惰性电极作阳极,铁作阴极,请写出阳极的电极反应式__________________。
(4)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液 d.氨水、酚酞试液
(5)废气中SO2与稀硫酸酸化的软锰矿反应的化学方程式为_______________;已知废气中SO2浓度为6.4g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000m3燃煤尾气,可得到硫酸锰晶体(MnSO4·H2O,相对分子质量为169)质量为_________________kg(结果保留3 位有效致字)。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上段考三化学试卷(解析版) 题型:选择题
已知热化学方程式:H2(g)+2ICl(g)=2HCl(g)+I2(g) △H = a kJ·mol-1。其反应过程如下:
①H2(g)+ICl(g)=HClI(g)+H(g) (慢)
②H(g)+ICl(g)=HCl(g)+I(g) (快)
③HClI(g)=HCl(g)+I(g) (快)
④I(g)+I(g)=I2(g) (快)
下列说法不正确的是( )
A.总反应的速率由反应①的速率决定
B.反应④的焓变小于0
C.HClI是上述总反应的催化剂
D.正反应活化能Ea1与逆反应活化能Ea2之差为a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:选择题
有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有四位同学为鉴别它们采用以下不同方 法,其中不可行的是( )
法,其中不可行的是( )
A.分别将它们 配制成溶液,再加入澄清石灰水
B.分别将它们配制成溶液,再逐滴加入等浓度的稀盐酸
C.分别将它们配制成溶液,再加入CaCl2溶液
D.分别加热,再用石灰水检验是否有CO2产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com