
| A. | 溶液的pH变小 | B. | 阴极逸出气体 | ||
| C. | 阳极附近溶液呈蓝色 | D. | 阴极附远溶液呈红色 |
分析 以石墨为电极,电解KI溶液时,在阴极上是氢离子得电子发生还原反应,阳极上是碘离子失电子发生氧化反应,据此回答判断.
解答 解:A、以石墨为电极,电解KI溶液时,生成氢氧化钾溶液,溶液的pH变大,故A错误;
B、以石墨为电极,电解KI溶液时,在阴极上是氢离子得电子发生还原反应逸出气体氢气,故B正确;
C、以石墨为电极,电解KI溶液时,阳极上是碘离子失电子发生氧化反应生成碘单质,遇到淀粉变蓝色,故C正确;
D、以石墨为电极,电解KI溶液时,在阴极上是氢离子得电子发生还原反应,该极区碱性增强,遇到酚酞溶液呈红色,故D正确;
故选A.
点评 本题考查学生电解池的工作原理以及物质的性质知识,注意知识的归纳和整理是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| Ⅰ操作 | Ⅱ结论 | |
| A | 滴加Ba(OH)2溶液生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加AgNO3溶液生成白色沉淀 | 原溶液中有Cl- |
| C | 滴加过量浓NaOH溶液并加热,将湿润红色石蕊试纸置于试管口,试纸变蓝色 | 原溶液中有NH4+ |
| D | 滴加氯水和CCl4,振荡、静置,上层溶液显紫红色 | 原溶液中有I- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用pH试纸测定溶液pH时若先润湿,测得溶液的pH一定有影响 | |
| B. | 25℃时,水溶液中水电离出的c(H+)和水电离的c(OH-)乘积一定等于10-14 | |
| C. | 如果Na2Y的水溶液显中性,该溶液中一定没有电离平衡 | |
| D. | 温度保持不变,向水中加入醋酸钠固体一定会影响水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
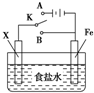
| A. | 若X为锌棒,开关K置于A处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 | |
| B. | 若 X 为锌棒,开关 K 置于 A 或 B 处均可减缓铁的腐蚀 | |
| C. | 若X为铜棒,开关K置于A处,装置中发生的总反应为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑ | |
| D. | 若X为碳棒,开关K置于B处,向食盐水中滴入酚酞溶液可看到铁棒附近先变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了防止蛋白质盐析,疫苗等生物制剂应冷冻保藏 | |
| B. | 污水处理可采用混凝法,明矾是一种常用的混凝剂 | |
| C. | 硅单质常作为制备光导纤维的主要材料 | |
| D. | 淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
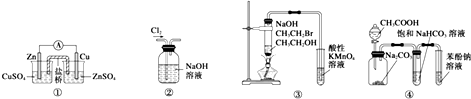
| A. | 装置①:构成锌-铜原电池 | |
| B. | 装置②:除去Cl2中含有的少量HCl | |
| C. | 装置④:由实验现象推知酸性强弱顺序为CH3COOH>H2CO3>C6H5OH | |
| D. | 装置③:验证溴乙烷发生消去反应生成烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cl2与足量Fe反应,转移的电子数为3NA | |
| B. | 1molNa2O2固体跟足量CO2气体完全反应,转移NA个电子 | |
| C. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| D. | 100mL 0.1mol/L盐酸中含HCl分子数为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中H+、NH4+、NO3-、Cl-可以大量共存 | |
| B. | Cu(NH3)4SO4中呈正四面体的原子团只有SO42- | |
| C. | 滴加Na2CO3溶液产生CuCO3蓝色沉淀 | |
| D. | 硫酸铜溶液与氨水作用后可缓缓加入乙醇可产生晶体,其产生晶体的主要原理是CuSO4+4NH3═[Cu(NH3)4]SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
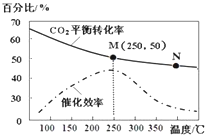
| A. | 生成乙烯的速率:v(M)一定小于v(N) | |
| B. | 化学平衡常数:KN>KM | |
| C. | 当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低 | |
| D. | 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com