
【题目】苯氧乙醇是护肤产品中常用的一种有机物,下图是利用烃M和苯酚为主要原料制备苯氧乙醇的合成路线,请回答相关问题。
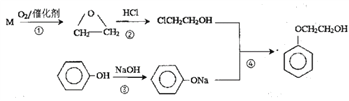
(1)反应①中M与氧气的物质的量之比为2:1且原子利用率为100%,则M的结构简式是_______________,反应①的反应类型是___________________。
(2)ClCH2CH2OH的名称是_____________________。
(3)苯氧乙醇中含有的官能团是___________________,分子式是___________________。
(4)苯酚除了与氢氧化钠反应外也可以与碳酸钠反应生成苯酚钠,该反应的化学方程式是_____________
(5)苯氧乙醇的同分异构体中符合下列要求的有__________种(不考虑一个碳原子上连两个羟基的情况)。
a.属于芳香化合物且苯环上有奇数个取代基
b.能与钠反应生成氢气且只含有一种官能团
其中核磁共振氢谱中峰的数目最少的结构简式为_________________________。
【答案】 CH2=CH2 氧化反应 2-氯乙醇 醚键、(醇)羟基 C8Hl0O2 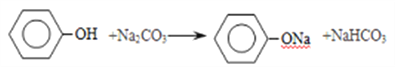 7
7 
【解析】 (1)反应①中M与氧气的物质的量之比为2:1且原子利用率为100%,则M为乙烯,其结构简式是CH2=CH2,反应①的反应类型是氧化反应。
(2)ClCH2CH2OH的名称是2-氯乙醇。
(3)苯氧乙醇中含有的官能团是醚键、(醇)羟基,分子式是C8Hl0O2。
(4)苯酚除了与氢氧化钠反应外也可以与碳酸钠反应生成苯酚钠,该反应的化学方程式是 。
。
(5)苯氧乙醇的同分异构体中符合下列要求:a.属于芳香化合物且苯环上有奇数个取代基;b.能与钠反应生成氢气且只含有一种官能团,说明分子中一定有羟基。这样的同分异构体的有:苯基乙二醇、3-乙基-1,2-苯二酚、4-乙基-1,2-苯二酚、2-乙基-1,3-苯二酚、3-乙基-1,3-苯二酚、4-乙基-1,3-苯二酚、2-乙基-1,4-苯二酚,共7种。其中核磁共振氢谱中峰的数目最少的结构简式为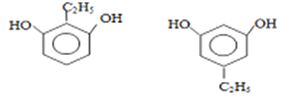 。
。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】有机物G是一种常用的植物调味油,工业上可按如下路线合成。
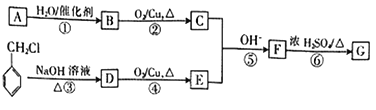
已知:
①有机物A是分子中单键与双键数目之比为4∶1的烯烃;
②G的分子式为C9H8O,能发生银镜反应;
③CH3CHO+CH3CHO![]()
![]() 。
。
回答下列问题:
(1)B的名称为__________,F中含有的官能团的名称是__________。
(2)E的结构简式为__________,G的结构简式为________________。
(3)⑤的反应类型为__________,⑥的反应类型为__________。
(4)反成③的化学方程式为_____________________________。
(5)反应①~⑥中符合原子经济性(原子利用率为100%)的是__________ (填序号)。
(6)同时符合下列条件的F的同分异构体有__________种,其中核磁共振氢谱显示有四组峰,且峰面积之比为3∶3∶2∶2的是__________ (填结构简式)。
a.苯环上含有两个取代基 b.分子中含有-COO-结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素中有N、P、As三种非金属元素,请回答下列相关问题。
(1)基态砷原子的价电子排布式为_________________,同周期元素原子中与其含有相同数目未成对电子的是___________________(填元素符号)。
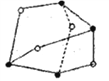
(2)雄黄(As4S4)是很多人熟悉的一种物质,其分子结构如图所示,分子中所有原子最外层均达到8电子结构。分子中含有的σ键的数目是__________________,●表示的原子是______________,该原子的杂化形式是____________________。
(3)硝酸的沸点较低,从氢键的角度推断其可能的原因是_______________________。硝酸根的空间构型是_____________________。
(4)白磷(P4)晶体中分子堆积方式属于分子密堆积,每个分子周围紧邻的分子有_________个。若白磷晶体晶胞的棱长为ypm,阿伏伽德罗常数的数值用NA表示,则白磷晶体的密度为____________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值, 下列有关叙述正确的是
A. 1 mol OH-所含电子数为10NA
B. 2 L 0.5 mol·L-1Na2SO4溶液中阴离子所带电荷数为0.2NA
C. 标准状况下,1.12 LH2O 含有的氢原子数为0.1NA
D. 14 g由CO和N2组成的混合气体中含有的分子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常认为残留在溶液中的离子浓度小于1×10-5mol/L时,离子不存在。图为H3PO4(图中用H3A表示)在加入强酸或强碱溶液后,平衡时溶液中各微粒浓度的对数值(lgc)-pH图。下列说法不正确的是( )
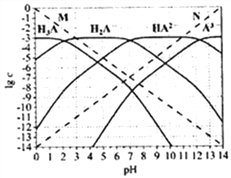
A. H3PO4、H2PO4-、HPO42-、PO43-不能在同一溶液中大量共存
B. H3PO4电离平衡常数Ka2≈1×10-7
C. 图中虚线M、N分别代表H+和OH-
D. pH=10时,溶液中存在关系:c(HPO42-)>c(OH-)>c(PO43-)>c(H2PO4-)>c(H3PO4)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况}。向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
A. 该合金中铜与铁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C. 得到2.54g沉淀时,加入NaOH溶液的体积是600mL
D. NO2和N2O4的混合气体中,NO2的体积分数是80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com