
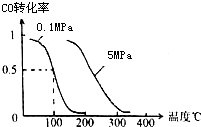
 (1)在一定条件下,容积为 100L密闭容器中发生反应:
(1)在一定条件下,容积为 100L密闭容器中发生反应:| △c |
| △t |
| c(CH3OH) |
| c(CO)?c3(H2) |
| ||
| 10min |
| 0.5a |
| VL |
| a |
| 2V |
| amol |
| VL |
| a |
| V |
| a |
| 2V |
| c(CH3OH) |
| c(CO)?c3(H2) |
| ||||
|
| V2 |
| a2 |
| V2 |
| a2 |
| 5.5mol |
| 2.5mol+7.5mol |


科目:高中化学 来源: 题型:
| A、SO3+H2O=H2SO4 | ||||
| B、CaCO3+2HCl=CaCl2+H2O+CO2↑ | ||||
| C、Cl2+H2O=HCl+HClO | ||||
D、2NaHCO3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯净的氯气是一种黄绿色、有毒的气体,具有漂白性 |
| B、可用干燥的石蕊试纸验证氯水是否变质 |
| C、氯气能与铁反应,液氯不宜贮存在钢瓶中 |
| D、氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将40g NaOH溶解于1L水中,得到1mol?L-1的NaOH溶液 |
| B、将11.2L HCl气体通入水中配成0.5L溶液,浓度为1mol?L-1 |
| C、将1L 10 mol?L-1的盐酸与9L水混合,混合液浓度为1mol?L-1 |
| D、10g NaOH溶解在水中配成250mL溶液,其浓度为1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 性质 | NO | NO2 |
| 沸点 | 21℃ | -152℃ |
| 与NaOH反应情况 | 不反应 | 2NO2+2NaOH═NaNO2+NaNO3+H2O |
| 备注 | NO+NO2+2NaOH═2NaNO2+H2O | |
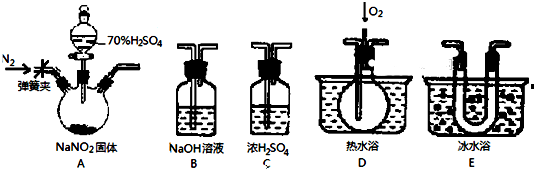
查看答案和解析>>
科目:高中化学 来源: 题型:
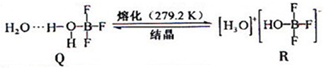
查看答案和解析>>
科目:高中化学 来源: 题型:
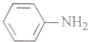 )具有
)具有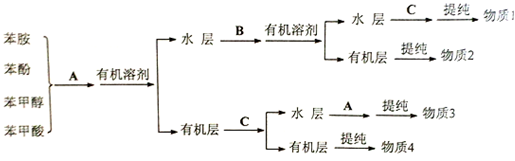
 转化为
转化为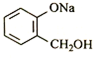 ,则应加入
,则应加入查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com