
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
下列说法不正确的是

A.在阴极式,发生的电极反应为:2H2O+2e- 2OH―+H2↑
2OH―+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2 +2H+
+2H+
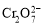 +H2O向右移动
+H2O向右移动
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O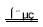 2K2Cr2O7+4KOH+2H2↑+2O2↑
2K2Cr2O7+4KOH+2H2↑+2O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=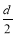
D
【解析】本题是电解法在制备物质中的具体应用。分析该制备时,重点要把握其中的K2CrO4在转变为K2Cr2O7的过程中没有发生化合价的变化,所以要抓住是由于溶液的pH变化实现目标物的合成,制备的过程是通过电解的方法改变溶液的pH来实现。阴极的反应是 2H2O+2e-=2OH-+H2,阳极为2H2O-4e-=O2+4H+,电解过程中阳极区的c(H+)增大,促进平衡2CrO42-+2H+= Cr2O72-+H2O向右移动,总反应为4 K2CrO4+4H2O=2 K2Cr2O7+4KOH+2H2↑+O2↑;若设加入反应容器内的K2CrO4有1mol,反应中有x mol K2CrO4转化为K2Cr2O7,则阳极区剩余的K2CrO4为(1-x) mol,对应的n(K)=2(1-x) mol,n(Cr)= (1-x) mol,生成的K2Cr2O7为x/2 mol,,对应的n(K)= x mol,n(Cr)= x mol,由n(K)/ n(Cr)=d可得,x=2-d,转化率为(2-d)/1。
【考点定位】本题通过制备重铬酸钾考查电化学知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014上海市宝山区高二年级化学学科质量监测化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A. 1mol O的质量是32 g/mol B. OH-的摩尔质量是17 g
C. 1mol H2O的质量是18 g/mol D. CO2的摩尔质量是44 g/mol
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(海南卷解析版) 题型:简答题
合成氨的流程示意图如下:
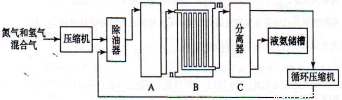
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是 , ;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式 , ;
(2)设备A中含有电加热器,触媒和热交换器,设备A的名称是 ,其中发生的化学反应方程式为 ;
(3)设备B的名称是 ,其中m和n是两个通水口,入水口是 (填“m”或“n”)。不宜从相反方向通水的原因是 ;
(4)设备C的作用是 ;
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过以下反应来实现:
CO(g)+H2O(g)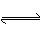 CO2(g)+H2(g)
CO2(g)+H2(g)
已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中的c(H2O):c(CO)不低于 。
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(海南卷解析版) 题型:选择题
分子式为C10H14的单取代芳烃,其可能的结构有
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(浙江卷解析版) 题型:简答题
[15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应过程 | 化学方程式 | 焓变△H (kJ/mol) | 活化能Ea (kJ/mol) |
甲烷氧化 | CH4(g)+2O2(g) | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸汽重整 | CH4(g)+H2O(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g) CO2(g)+H2(g)的△H= kJ/mol。
CO2(g)+H2(g)的△H= kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)的KP= ;
CO(g)+3H2(g)的KP= ;
随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量阶段分析,甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:

①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
A.600℃,0.9MpaB.700℃,0.9MPaC.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始即时)
的变化趋势示意图:

(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是 。
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(新课标解析版) 题型:简答题
【选修3物质结构与性质】(15分)
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是 ;

(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离
子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为 ;
(3)Se原子序数为 ,其核外M层电子的排布式为 ;
(4)H2Se的酸性比H2S (填“强”或“弱”)。气态SeO3分子的立体构型
为 ,SO32-离子的立体构型为 ;
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,
K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:
;
② H2SeO4比 H2SeO3酸性强的原因:
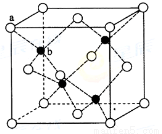
(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm.密度为 (列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为 pm(列示表示)
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(新课标解析版) 题型:选择题
已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1 的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的PH=7
C.混合溶液中,c(H+)= 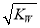 mol.L-1
mol.L-1
D.混合溶液中c(H+)+c(B+)=c(OH-)+C(A-)
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(山东卷解析版) 题型:填空题
(13分)(2012?山东)[化学﹣有机化学基础]
合成P(一种抗氧化剂)的路线如下:
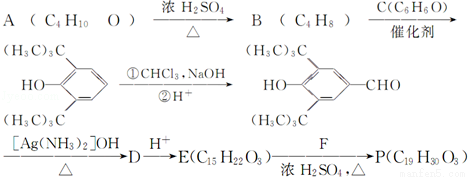
已知:①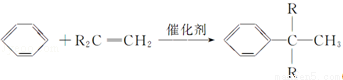 (R为烷基);
(R为烷基);
②A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基.
(1)A→B的反应类型为 .B经催化加氢生成G(C4H10),G的化学名称是 .
(2)A与浓HBr溶液一起共热生成H,H的结构简式为 .
(3)实验室中检验C可选择下列试剂中的 .
a.盐酸 b.FeCl3溶液
c.NaHCO3溶液 d.浓溴水
(4)P与足量NaOH溶液反应的化学反应方程式为 (有机物用结构简式表示).
查看答案和解析>>
科目:高中化学 来源:2012-2014四川省宜昌市春季期中考试高一化学试卷(解析版) 题型:选择题
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大。X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层电子数与其电子层数相等,Z—与M2+具有相同的核外电子层结构。下列推测正确的是 ( )
A.原子半径Y>Z,离子半径Z—<M2+
B.MX2与水发生反应时,MX2只做氧化剂
C.X、Y形成的化合物既能与强酸反应又能与强碱反应
D.MX2、MZ2两种化合物中,都含有离子键和共价键,且阳离子与阴离子个数比均为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com