

A.A是盐酸,B是NaOH,且c(NaOH)=2c(HCl)
B.原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=1∶1∶5
C.A是NaOH,B是盐酸,且c(NaOH)∶c(HCl)=2∶1
D.从6到9,相应离子反应方程式为:H++OH-====H2O
A
解析:根据加入前6 mL试剂时,先有沉淀生成而后溶解,所以,试剂A是NaOH,则B是盐酸,A选项错误。
从加入5 mL A生成沉淀最多,再继续加1 mL A沉淀量减少到最小值,相应反应的离子方程式为:Al(OH)3+OH-====![]() +2H2O,由此可知,n(Al3+)=n〔Al(OH)3〕=(1×6×10-3) mol;
+2H2O,由此可知,n(Al3+)=n〔Al(OH)3〕=(1×6×10-3) mol;
由前5 mL NaOH形成最大沉淀量可知,2n(Mg2+)+3n(Al3+)=(5×10-3×6) mol;
即溶液中c(Mg2+)∶c(Al3+)∶c(Cl-)=1∶1∶5,B选项正确。
又由图可知,5→6(1 mL)、9→11(2 mL)分别是溶解Al(OH)3和使![]() 恰好完全生成Al(OH)3沉淀消耗的NaOH和HCl。根据铝元素守恒:
恰好完全生成Al(OH)3沉淀消耗的NaOH和HCl。根据铝元素守恒:
NaOH—Al(OH)3—![]() —H+
—H+
1 1 1 1
由此可以推出:c(NaOH)∶c(HCl)=2∶1,C选项正确。
由6 mL和9 mL对应液体中沉淀量相等,可以推知此时仅仅发生酸碱中和反应,即H++OH-====H2O,故D选项正确。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
 某同学设计了如下两种制备氢氧化铝的方案:
某同学设计了如下两种制备氢氧化铝的方案:| 100mL盐酸 |
| NaOH溶液 |
| 100mLNaOH |
| HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
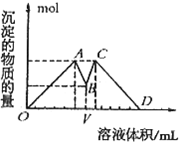 如图所示是向MgCl2、AlCl3混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论不正确的是( )
如图所示是向MgCl2、AlCl3混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论不正确的是( )| A、混合溶液中c(AlCl3):c(MgCl2)=1:1 | B、混合溶液中c(AlCl3):c(MgCl2)=3:1 | C、V之前加NaOH溶液,V之后加盐酸 | D、这种盐酸与NaOH溶液中溶质的物质的量浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如右图所示为向MgCl2、AlCl3的混合溶液中,开始滴加b mol·L-1试剂A,之后改滴试剂B,所得沉淀y(mol)与试剂体积V(mL)间的关系。以下结论不正确的是( )
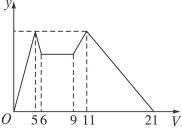
A.A是盐酸,B是NaOH,且c(NaOH)=2c(HCl)
B.原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=1∶1∶5
C.A是NaOH,B是盐酸,且c(NaOH)∶c(HCl)=2∶1
D.从6到9,相应离子反应方程式为:H++OH-====H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com