
| A. | O2和O3互为同位素 | |
| B. | O2和O3的相互转化是化学变化 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | 等物质的量O2和O3含有相同的质子数 |
分析 A.同种元素的不同单质为同素异形体;
B.有新物质生成的变化属于化学变化;
C.由同种元素组成的纯净物是单质;
D.等质量的氧气和臭氧,其物质的量之比等于其摩尔质量反比,其分子个数之比等于其摩尔质量反比,再结合分子构成判断.
解答 解:A.同种元素的不同单质为同素异形体,氧气和臭氧属于同素异形体,故A错误;
B.臭氧和氧气之间的转化过程中有新物质生成,属于化学变化,故B正确;
C.由同种元素组成的纯净物是单质,臭氧分子是由3个O原子构成,臭氧属于单质,故C错误;
D.等质量的氧气和臭氧,其物质的量之比等于其摩尔质量反比为3:2,其分子个数之比等于物质的量之比为3:2,每个臭氧分子中含有3个O原子、每个氧气分子中含有2个O原子,所以其含有原子个数相等,故D错误.
故选B.
点评 本题以氧气和臭氧为载体考查了基本概念、物质的量的计算等知识点,根据同素异形体、单质、化学变化等基本概念及物质的量的计算来分析解答,注意同素异形体、同位素、同分异构体的区别,题目难度不大.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:选择题
| A. | 两者均属于离子化合物 | |
| B. | 两种化合物中所含有化学键类型相同 | |
| C. | Na3N与盐酸反应可得到2种盐 | |
| D. | Na3N中N3-半径比Na+半径大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该有机物分子中不含有氧原子 | |
| B. | 该有机物分子中含一个氧原子 | |
| C. | 该有机物一个分子中含2个氧原子 | |
| D. | 不能确定该有机物分子中是否含有氧原子及其个数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与乙烯共1mol,完全燃烧后生成的H2O为2mol | |
| B. | 光照下,异丁烷与Cl2发生取代反应生成的一氯代物有三种 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,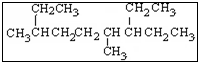 名称:4,7-二甲基-3-乙基壬烷 名称:4,7-二甲基-3-乙基壬烷 | |
| B. | 元素分析仪可以同时对碳、氢、氧、硫等多种元素进行分析 | |
| C. | 用相同浓度的乙醇和苯酚水溶液,分别与相同质量的金属钠反应,来比较两者羟基上氢的活性 | |
| D. | 等质量的下列物质燃烧耗O2量:乙炔>乙烯>乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中 | 试管A中不再产生气泡 试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液 | 试管A、B中均未见气泡产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com