
Ⅰ.图1是某压强下工业合成氨生产过程中,N2与H2按体积比为1:3投料时,反应混合物中氨的体积分数随温度的变化曲线,其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。
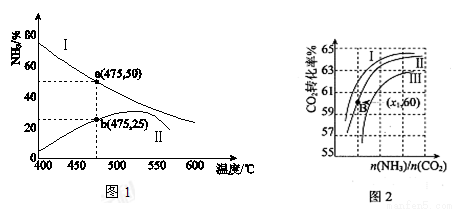
(1)图中表示该反应的平衡曲线的是__________(填“Ⅰ”或“Ⅱ”);由图中曲线变化趋势可推知工业合成氨的反应是___________(填“吸热”或“放热”)反应。
(2)图中a点,容器内气体n(N2):n(NH3)= ____________,图中b点,v(正)_________v(逆)(填“>”、“=”或“<”)。
Ⅱ.以工业合成氨为原料,进一步合成尿素的反应原理为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)
CO(NH2)2(l)+H2O(g)
工业生产时,需要原料气带有水蒸汽,图2中曲线I、Ⅱ、Ⅲ表示在不同水碳比[n(H2O)/n(CO2)]时,CO2的转化率与氨碳比[n(NH3)/n(CO2)]之间的关系。
(1)写出该反应的化学平衡常数表达式____________________
(2)曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是_________,判断依据是_______________
(3)测得B点氨的转化率为40%,则x1=__________。
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:2016届广东省顺德市高三上第四次月考理综化学试卷(解析版) 题型:选择题
X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。
下列说法正确的是
A.室温下,0.1 mol/L W的气态氢化物的水溶液的pH >1
B.Z的最高价氧化物能与水反应生成相应的酸
C.Y单质在一定条件下可以与氧化铁发生置换反应
D.原子半径由小到大的顺序:X<Y<Z<W
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期月考化学试卷(解析版) 题型:选择题
某无色溶液中只可能含有Na+ 、Ba2 +、Mg2+、Cl一、Br一、SO32一、SO42一,对该溶液进行下列实验,实验操作和现象如下表:
步骤 | 操 作 | 现 象 |
(1) | 取少量溶液滴加几滴石蕊试液 | 溶液变蓝 |
(2) | 另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 | 上层无色,下层呈橙红色 |
(3) | 取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 | 有白色沉淀产生 |
(4) | 向(3)的滤液中加入过量AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是
A.可能含有 Cl一、Mg2+、SO42一
B.肯定含有 Na+、Br-、SO32-
C.肯定没有 Ba2+、Br-、Cl-
D.不能确定 Mg2+ 、SO32-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是
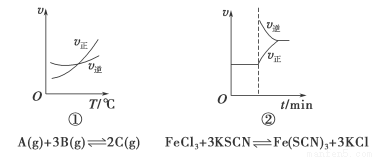
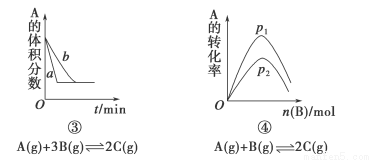
A.①是其他条件一定时,反应速率随温度变化的图像,正反应ΔH<0
B.②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C.③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次月考化学试卷(解析版) 题型:选择题
下列对一些实验事实的理论解释正确的是
选项 | 实 验 事 实 | 理 论 解 释 |
A. | SO2溶于水形成的溶液能导电 | SO2是电解质 |
B. | 白磷为正四面体分子 | 白磷分子中P-P间的键角是109°28′ |
C. | 1体积水可以溶解700体积氨气 | 氨是极性分子且由于有氢键的影响 |
D. | HF的沸点高于HCl | H-F的键长比H-Cl的键长短 |
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上四次模拟化学卷(解析版) 题型:选择题
化学与生活、科学、技术、社会、环境密切相关,下列有关说法中错误的是
A .高纯硅可作计算机芯片的材料
B.洁厕灵的主要成分是盐酸,不能与“84”消毒液(主要成分是NaClO)混用
C.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体
D.Na2SiO3溶液可做木材防火剂
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:填空题
工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3),具体生产流程如下:
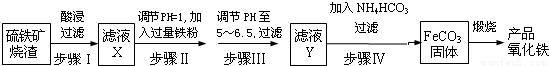
试回答下列问题:
(1)滤液X中含有的金属阳离子是______________(填离子符号)。
(2)步骤Ⅲ中可选用________调节溶液的pH(填字母)。
A.稀硫酸 B.氨水
C.氢氧化钠溶液 D.高锰酸钾溶液
(3)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是______________。
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是__________________________。
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二普通班上期中化学试卷(解析版) 题型:选择题
HA为酸性略强于醋酸的一元弱酸.在0.1mol•L﹣1NaA溶液中,离子浓度关系正确的是( )
A.c(Na+)>c(A﹣)>c(H+)>c(OH﹣)
B.c(Na+)>c(OH﹣)>c(A﹣)>c(H+)
C.c(Na+)+c(H+)=c(A﹣)+c(OH﹣)
D.c(Na+)+c(OH﹣)=c(A﹣)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附中高一下第一次段考化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A. 在钠、钾、铷三种单质中,钠的熔点最高
B. 所有碱金属均为银白色
C. 同一主族卤素单质从上到下熔沸点依次升高
D. 液溴易挥发,可以通过水封的方式进行保存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com