
| A、4.6 g乙醇分子中含有碳氢键的数目为0.6NA | B、1 mo1C12与足量Fe反应,转移的电子数为3NA | C、由CO2和O2组成的混合物中共有NA个分子,其中所含的氧原子数必为2NA | D、28 gC16O与28 gC18O中含有的质子数均为14 NA |
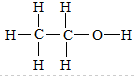 ,乙醇分子中含有5个碳氢键,乙醇的摩尔质量为46g/mol,4.6g乙醇的物质的量为0.1mol,含有0.5mol碳氢键;
,乙醇分子中含有5个碳氢键,乙醇的摩尔质量为46g/mol,4.6g乙醇的物质的量为0.1mol,含有0.5mol碳氢键;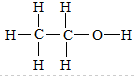 可知,0.1mol乙醇含有0.5mol碳氢键,含有碳氢键的数目为0.5NA,故A错误;
可知,0.1mol乙醇含有0.5mol碳氢键,含有碳氢键的数目为0.5NA,故A错误;| m |
| M |


科目:高中化学 来源: 题型:
| A、6.8g熔融的KHSO4中含有阳离子数0.05 NA | B、1mol冰醋酸和1mol乙醇经催化加热反应可生成H2O分子数为NA | C、25℃时,pH=13的Ba(OH)2溶液中含有的OH-数为0.1 NA | D、常温常压下,17 g羟基中含有的电子数为9 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L CCl4中含有的分子数目大于NA | B、3.4g NH3中含N-H键数目为0.2NA | C、1L 0.1mol?L-1乙酸溶液中H+数为0.1NA | D、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,46gN02与N204的混合气体中含有的原子数为3NA | B、15.6 g Na2O2与过量CO2反应时,转移的电子数为O.4NA | C、常温常压下,11.2L 二氧化硫中所含的氧原子数等于NA | D、1L 1 mol?L-1 的Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,0.56L丙烷中含有共价键数为0.2NA | B、常温常压下,3.2g氧气和臭氧的混合气体中含有的原子数为0.2NA | C、常温下,5.6g铁与一定量浓硫酸恰好反应,转移的电子数一定为0.2NA | D、25℃,1L pH=12的氨水中含有的OH-离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,18g H218O中含有的原子数小于3NA | B、标准状况下,22.4L HF中含有的氟原子数目为NA | C、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | D、4.6g Na与O2反应生成Na2O和Na2O2,转移电子数介于0.1NA~0.2NA之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L0.5mol?L-1的(NH4)2SO4溶液中含NH4+ 数为NA | B、常温常压下,1molCH4中含有4NA个C-H键 | C、常温常压下,48g O3含有原子数为2NA(相对原子质量:O 16) | D、标准状况下,22.4LC6H6(苯)的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,46 g NO2和N2O4的混合气体中含有NA个氮原子 | B、常温常压下,NA个铝原子与足量NaOH溶液反应生成33.6 L H2 | C、1 L 1 mol?L-1的Na2CO3,溶液中含有Na+、CO32-共3NA个 | D、25℃时,1 L pH=1的H2SO4溶液中含有0.2NA个H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
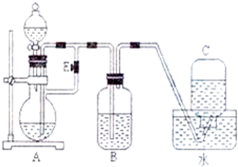 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及5.00mol?L-1的硫酸,其他试剂任选.填写下列空白:
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化,实验时必须使用铁屑及5.00mol?L-1的硫酸,其他试剂任选.填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com