
分析 (1)体积之比等于物质的量之比可计算反应后的气体的物质的量,结合三段式法计算该题.
(2)起始时加入amolS02、b mol O2,且a:b=2:l,在同样温度和压强下,反应达到平衡时,与(1)平衡状态相同,为等效平衡,物质的转化率和百分含量都相同,SO3的体积分数为与(1)相同,结合体积的关系计算;
(3)若将密闭容器体积固定为100L,起始时加入xmolS02、y mol 02和z mol SO3,反应达平衡时,温度、压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,为等效平衡.
解答 解:(1)反应方程式为2SO2+O2?2SO3,利用三段式计算,
2SO2+O2?2SO3
起始:2mol 1mol 0
转化:2x x 2x
平衡:1.6-2x 0.8-x 2x
根据体积之比等于物质的量之比可知:(1.6-2x+0.8-x+2x):2.4=80:100,
解之得x=0.48,反应的气体的物质的量为:1.6-0.48×2+0.8-0.48+0.48×2=1.92mol,
所以SO2的转化率为$\frac{0.48×2}{1.6}$×100%=60%,
故答案为:60%;
(2)起始时加入amolS02、b mol O2,且a:b=2:l,在同样温度和压强下,反应达到平衡时,与(1)平衡状态相同,为等效平衡,物质的转化率和百分含量都相同,SO3的体积分数为与(1)相同,
2SO2+O2 ?2SO3
起始:amol bmol 0
转化:0.6a 0.3a 0.6a
平衡:a-0.6a b-0.3a 0.6a
压强之比就等于物质的量之比,列式为:$\frac{a-0.6a+b-0.3a+0.6a}{1.92}$=$\frac{120}{80}$,a=2b,
解得:a=2.4mol,b=1.2mol,
故答案为:2.4;1.2;
(3)若将密闭容器体积固定为100L,起始时加入xmolS02、y mol 02和z mol SO3,反应达平衡时,温度、压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,为等效平衡,则有x=2y,且相当于只加二氧化硫和氧气时,起始时二氧化硫的物质的量为x,$\frac{x}{100}$=$\frac{2.4}{120}$,x=2,即:x+z=2,
故答案为:x=2y;x+z=2.
点评 本题考查化学平衡的计算、等效平衡判断等知识,题目难度较大,注意等效平衡状态的判断及应用,明确恒温恒压、恒温恒容条件下的等效平衡的特点,试题充分考查了学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
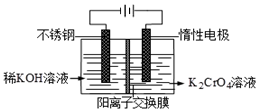 已知重铬酸钾(K2Cr2O7)是一种中学实验室常用的强氧化剂.重铬酸钾溶液中存在以下平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙红色)+H2O.
已知重铬酸钾(K2Cr2O7)是一种中学实验室常用的强氧化剂.重铬酸钾溶液中存在以下平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙红色)+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、石膏 | B. | 盐酸、烧碱、胆矾 | ||
| C. | HNO3、乙醇、氯化钠 | D. | H3PO4、熟石灰、苛性钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
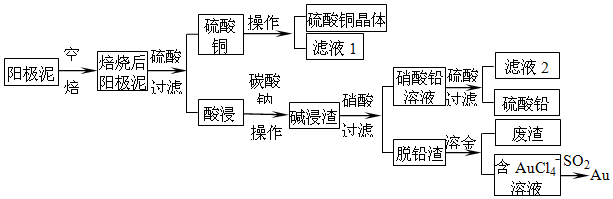
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 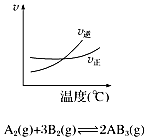 如图说明此反应的正反应是吸热反应 | |
| B. | 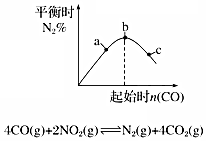 如图说明NO2的转化率b>a>c | |
| C. |  如图说明反应至15 min时,改变的条件是升高温度 | |
| D. |  如图说明生成物D一定是气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com