
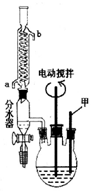
 苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下:
苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下:分析 (1)反应需要保持温度,仪器甲为温度计;
(2)甲苯在硫酸的作用下被高锰酸钾氧化为苯甲酸,高锰酸钾被还原为硫酸锰;
(3)抽滤速度快,得到的固体水分少;
(4)产品表面有氯离子,检验洗涤液中是否混有氯离子即可;沸水浴上干燥;
(5)计算18.4g甲苯理论上生成的苯甲酸质量,再计算产率;
(6)a mol苯甲酸和b mol KOH混合加水形成2L溶液,测得溶液的pH=7,则c(K+)=c(C6H5COO-)>c(H+)=c(OH-),c(K+)=$\frac{b}{2}$mol/L,c(C6H5COO-)=$\frac{b}{2}$mol/L,由物料守恒可得c(C6H5COOH),由此计算苯甲酸的Ka.
解答 解:(1)反应温度在90℃左右,仪器甲为温度计;
故答案为:温度计;
(2)甲苯在硫酸的作用下被高锰酸钾氧化为苯甲酸,高锰酸钾被还原为硫酸锰,反应为:5C6H5CH3+6KMnO4+9H2504$\stackrel{90}{→}$5C6H5COOH+3K2SO4+6MnSO4+14H2O;
故答案为:5C6H5CH3+6KMnO4+9H2504$\stackrel{90}{→}$5C6H5COOH+3K2SO4+6MnSO4+14H2O;
(3)抽滤的优点是过滤速度快,得到的固体水分少;
故答案为:过滤速度快,得到的固体水分少;
(4)产品表面有氯离子,检验洗涤液中是否混有氯离子即可,方法我饿:取最后一次的洗涤液中滴加硝酸银溶液,若无沉徒生成,则说明沉淀洗涤干净了;沸水浴干燥较快,同时防止苯甲酸升华变质,故用沸水浴上干燥;
故答案为:取最后一次的洗涤液中滴加硝酸银溶液,若无沉徒生成,则说明沉淀洗涤干净了;b;
(5)18.4g甲苯物质的量为0.2mol,则理论生成的苯甲酸也为0.2mol,质量为0.2mol×122g/mol=24.4g,故产率为$\frac{23.4}{24.4}×100%$=95.9%;
故答案为:95.9%;
(6)a mol苯甲酸和b mol KOH混合加水形成2L溶液,c(K+)=$\frac{b}{2}$mol/L,测得溶液的pH=7,c(H+)=c(OH-),根据电荷守恒:c(K+)+c(H+)=c(C6H5COO-)+c(OH-),故c(K+)=c(C6H5COO-)=$\frac{b}{2}$mol/L>c(H+)=c(OH-)=10-7mol/L;
根据物料守恒:c(C6H5COO-)+c(C6H5COOH)=$\frac{a}{2}$mol/L,故c(C6H5COOH)=$\frac{a}{2}$mol/L-$\frac{b}{2}$mol/L,则苯甲酸的Ka=$\frac{c({C}_{6}{H}_{5}CO{O}^{-})•c({H}^{+})}{c({C}_{6}{H}_{5}COOH)}$=$\frac{\frac{b}{2}•1{0}^{-7}}{\frac{a}{2}-\frac{b}{2}}$=$\frac{b×1{0}^{-7}}{a-b}$,
故答案为:$\frac{b×1{0}^{-7}}{a-b}$; c(K+)=c(C6H5COO-)>c(H+)=c(OH-).
点评 本题以物质的制备为背景,涉及实验操作、物质的分离、离子检验、溶液中的离子平衡等知识点,注意阅读题给信息并充分利用信息进行解答,难度较大.


科目:高中化学 来源: 题型:解答题
 (1)如图Ⅰ所示,装置的B极上有大量气泡逸出,则B极是正(填“正”或“负”,下同)极
(1)如图Ⅰ所示,装置的B极上有大量气泡逸出,则B极是正(填“正”或“负”,下同)极查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 1 mol•L-1 Na2CO3溶液中含有NA个C原子 | |
| B. | 标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA | |
| C. | 常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 侯氏制碱法是将二氧化碳和氨气先后通入饱和氯化钠溶液中,制得碳酸氢钠固体,再在高温下灼烧,转化为碳酸钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该物质分子式为C16H12 | |
| B. | 该物质与甲苯互为同系物 | |
| C. | 该物质能与溴水发生取代反应和加成反应 | |
| D. | 该物质苯环上七氯代物的同分异构体有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素的有关叙述正确的是( )| A. | 分子式为C15H13O7 | |
| B. | 1 mol儿茶素A在一定条件下最多能与7molH2加成 | |
| C. | 等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应,消耗金属钠和氢氧化钠的物质的量之比为1:1 | |
| D. | 1 mol儿茶素A与足量的浓溴水反应,最多消耗Br24 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -个苯环上已经连有-CH3、-CH2CH3、-OH三种基团,如果在苯环上再连接一个-CH3,其同分异构体有16种 | |
| B. | 裂化汽油可用于萃取溴水中的溴 | |
| C. | 除去乙醇中的少量水,方法是加入新制生石灰,经过滤后即得乙醇 | |
| D. | 除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量烧碱溶液,通过分液即得乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋可用于除去暖水瓶中的水垢 | B. | 单质硅可用作光缆 | ||
| C. | 酒精可用于杀菌消毒 | D. | 纯碱可除去灶具上的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验方案 | 实验现象 | 实验结论 |
| A | 将一块铝片直接放入硫酸铜溶液中 | 短期内铝片表面无明显现象 | 铝不能置换出硫酸铜中的铜 |
| B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
| C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 有气泡产生 | Na2O2没有变质 |
| D | 将石蜡油、碎瓷片放入硬质试管中加强热,并将产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 在炽热瓷片的作用下,石蜡油发生了裂化、裂解反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com