
【题目】请回答氯碱工业中的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求写出计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是 (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
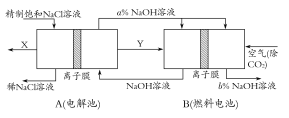
①图中X、Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应,正极: ;负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
【答案】(1)k=Mr(Cl2)/2Mr(NaOH)=71/80=1∶1.13或0.89
(2)③①②
(3)①Cl2 H2 a%<b%
②O2+4e-+2H2O=4OH- H2-2e-+2OH-=2H2O
③燃料电池可以补充电解池消耗的电能 提高产出碱液的浓度,降低能耗(其他合理答案也可)
【解析】(1)据化学方程式2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑即可计算出k值.
2NaOH+H2↑+Cl2↑即可计算出k值.
(2)把Na2CO3放在BaCl2之后,以除去过量的Ba2+;把盐酸放在NO2CO3之后,以除去过量的CO32-。
(3)判断出二极是解答二池问题的前提:燃料电池中通空气(氧化剂)的一极应为正极,所以:①Y(通入负极,还原剂)必为H2,继而H2产生于电解池的阴极,可推出产生于电解池阳极的X必为Cl2;a% NaOH进入燃料电池,出来后的浓度变化可用二种方法判断:[方法一]从Na+的移动方向来定:Na+向阴极(即正极)移动,所以正极b% NaOH浓度增大,负极流出的NaOH变稀;[方法二]从水、OH-的量变来定:负极H2-2e-+2OH-=2H2O,水增多、OH-减少,变稀;正极O2+4e-+2H2O=4OH-,水减少、OH-增多,所以正极增浓,即a<b。


科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图。下列说法正确的是(己知6Fe2++ Cr2O72-+14H+=6Fe3++2Cr3++7H2O)
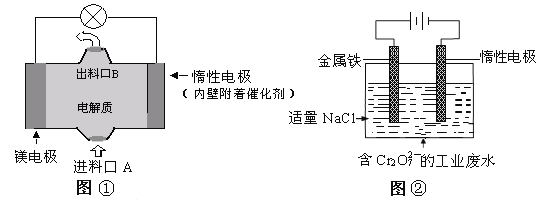
A. 图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B. 图②中阳极上的电极反应式为:Fe-3e-=Fe3+
C. 图①中发生的还原反应是:ClO-+H2O+2e-=Cl-+2OH-
D. 若图①中7.2g镁溶解产生的电量用以图②废水处理,理论可产生32.1g氢氧化铁沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是

A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g) ![]() 3Z(g) H<0
3Z(g) H<0
C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品,易溶于水,遇酸易分解,Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成。工业制备Na2S2O3的反应为: S(s)+Na2SO3(aq)![]() Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。
Na2S2O3(aq),产品中常含有少量Na2CO3 、 Na2SO3和Na2SO4。实验室拟用如下实验装置在C中制备Na2S2O3。

请回答下列问题:
(1)按如图所示装置进行实验,装置A中反应的化学方程式是______________________。装置C中可观察到溶液先变浑浊,后又澄清,生成的浑浊物质化学式为___________。
(2)装置B的作用为_________;为保证Na2S2O3的产量,实验中通入的SO2不能过量,原因是_________。
(3)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:

①实验装置的连接顺序依次________________(填装置的字母代号),装置C中的试剂为____________。
②能证明固体中含有碳酸钠的实验现象是__________________。
(4)若要检验固体硫代硫酸钠工业产品中含有Na2SO3,需先加水配成稀溶液,再依次加入的试剂为_____________________和品红溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存而且为无色透明的溶液是( )
A.NH4+、Al3+、SO42﹣、NO3﹣
B.K+、Na+、NO3﹣、CO32﹣
C.K+、MnO4﹣、NH4+、NO3﹣
D.H+ , K+ , OH﹣ , NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按酸、碱、盐、有机物、混合物顺序排列的是( )
A. 硝酸、苛性钠、明矾、淀粉、氯水
B. 碳酸钠、盐酸、食盐、酒精、合金
C. 醋酸、纯碱、碳酸钙、硝基苯、石油
D. 氢溴酸、消石灰、高锰酸钾、福尔马林、石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断中一定正确的是( )
A. NaCl及Na2O2固体中阴、阳离子数之比均为1:1
B. 等质量的O2与O3中,氧原子的个数比为3:2
C. 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2
D. 10 mL 0.3 mol·L-1 NaCl溶液与30 mL 0.1 mol·L-1 AlCl3溶液中Cl -物质的量浓度比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
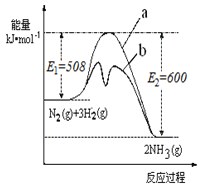
(1)根据如图提供的信息,写出该反应的热化学方程式 ,下图的曲线中 (填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达
平衡的是 。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | 1/3 | 10 | |
ⅲ | 480 | 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com