
【题目】能使带火星的木条复燃的气体是( )
A. O2 B. CO
C. N2 D. CO2
科目:高中化学 来源: 题型:
【题目】
氯吡格雷是一种血小板聚集抑制剂,该药物以![]() 为原料的合成路线如图:
为原料的合成路线如图:
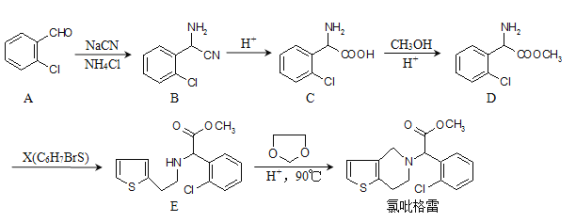
请根据以上信息,结合自己掌握的知识和具有的经验回答下列问题:
(1)分子C中无氧官能团的名称为____________。 命名为__________。
命名为__________。
(2)D→E的反应类型是_________反应。
(3)X的结构简式为___________________。
(4)下列叙述正确的是________(填序号)。
A.A物质中所有原子均可共面 B.C物质可发生取代、氧化、还原反应
C.![]() 在水中溶解度小 D.E中有两个手性碳原子
在水中溶解度小 D.E中有两个手性碳原子
(5)分子C在一定条件下生成一种含有3个六元环的产物的化学方程式为_____________。
(6)同时满足下列两个条件的B的同分异构体共有_____种(不包括B)。
①与B含有相同的官能团;②苯环上的取代基不超过2个。
(7)已知:![]() ,则由乙醇、甲醇为有机原料制备化合物
,则由乙醇、甲醇为有机原料制备化合物![]() 需要经历的反应类型有______(填序号)。
需要经历的反应类型有______(填序号)。
①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应
写出制备化合物![]() 的最后一步反应:______________________。
的最后一步反应:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.原子晶体中可能存在极性共价键
B.干冰升华时分子内共价键发生断裂
C.原子晶体的熔点比分子晶体的熔点低
D.离子晶体中只含离子键,不含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36g.cm-3。实验室制备少量1-溴丙烷的主要步骤如下:
步骤1:在仪器A中加入搅拌磁子、12g正丙醇及20mL水,冰水冷却下缓慢加入28mL浓H2SO4;冷却至室温,搅拌下加入24gNaBr。
步骤2:如上图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12mLH2O、12mL5%Na2CO3溶液和12mLH2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
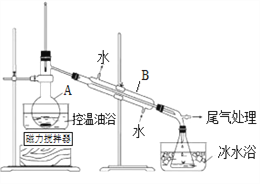
(1)仪器A、B的名称分别是____________________ 、______________________。
(2)反应时生成的主要有机副产物有_______________。(写出两种物质的结构简式)
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是_____________。
(4)写出生成1-溴丙烷的化学方程式_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017·新课标Ⅲ]砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________________________。
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ ![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ ![]() O2(g)=As2O5(s) ΔH3
O2(g)=As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:![]() (aq)+I2(aq)+2OH(aq)
(aq)+I2(aq)+2OH(aq)![]()
![]() (aq)+2I(aq)+ H2O(l)。溶液中c(
(aq)+2I(aq)+ H2O(l)。溶液中c(![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
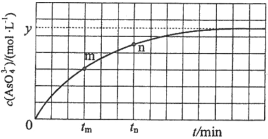
①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(![]() )
)
c.c(![]() )/c(
)/c(![]() )不再变化
)不再变化
d.c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. BaCrO4(s)![]() Ba2+(aq)+CrO42-(aq)的平衡体系中,加入BaCl2浓溶液沉淀量增多
Ba2+(aq)+CrO42-(aq)的平衡体系中,加入BaCl2浓溶液沉淀量增多
B. pH=2的酸溶液与pH=12的强碱溶液等体积混合,所得溶液pH≤7
C. 苯酚显色原理为:6C6H5OH+Fe3+![]() Fe(C6H5O)63-(紫色)+6H+,则检验水杨酸(
Fe(C6H5O)63-(紫色)+6H+,则检验水杨酸(![]() )中的酚羟基,需加入适量的小苏打溶液后,再加入氯化铁溶液
)中的酚羟基,需加入适量的小苏打溶液后,再加入氯化铁溶液
D. 某试液中加入盐酸酸化的氯化钡溶液有白色淀淀,该试液中一定含有SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中某区域的一些元素通常用来制造农药,这些元素是( )
A. 左下方区域的金属元素 B. 金属元素和非金属元素分界线附近的元素
C. 稀有气体元素 D. 右上方区域的非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A. 同周期元素中,ⅦA族元素的原子半径最大
B. ⅥA族元素的原子,其半径越大,越容易得到电子
C. 室温时,0族元素的单质都是气体
D. 元素周期表中,从ⅢB到ⅡB这10个纵行的元素都是副族元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com