
| A、至少存在4种离子 |
| B、Cl-一定存在,且c(Cl-)≥0.4mol/L |
| C、SO42-、NH4+、一定存在,Cl-可能不存在 |
| D、CO32-、Al3+一定不存在,K+可能存在 |
| 0.04mol |
| 0.1L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
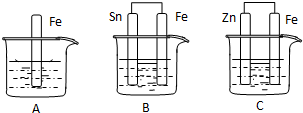 如图所示,烧杯中都盛有稀硫酸.
如图所示,烧杯中都盛有稀硫酸.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L |
| B、该混合物中不含Ba2+、Mg2+ |
| C、一定存在NH4+、K+,无法确定Cl-是否存在 |
| D、实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L酒精含有的分子数为 NA |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.01 NA |
| C、11.2 L H2所含的电子数为NA |
| D、通常状况下,NA个CO2分子含有原子数为3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+Ag+ Ba 2+ A13+Fe3+ |
| 阴离子 | OH - C1- SO42-NO3- CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com