
【题目】有关物质与反应分类的下列说法中,正确的是 ( )
A. 碳酸钠使无色酚酞试液变红,属于碱 B. CO2溶于水能导电,属电解质
C. 硅酸钠是钠盐,也是硅酸盐 D. CO还原氧化铁获得铁,属于置换反应
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】如图是某学校购买的硫酸试剂标签上的部分内容.据此下列说法正确的是( )

A. 该硫酸的物质的量浓度为1.84mol/L
B. 1mol Zn与足量的该硫酸反应产生2gH2
C. 配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL
D. 该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是
CH3OH(g)。在体积一定的密闭容器中按物质的量之比1∶2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示。现有两个体积相同的恒容密闭容器甲和乙,向甲中加入1mol CO和2 molH2,向乙中加入2 molCO和4molH2, 测得不同温度下CO的平衡转化率如图2所示。下列说法正确的是

A. 该反应的ΔH> 0; P1> P2 B. 反应速率B点高于D点
C. A、C两点的平衡常数相同 D. M、L两点中,CH3OH的体积分数相同,且p(M)= 2p(L)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1molL-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图 所示。下列判断正确的是
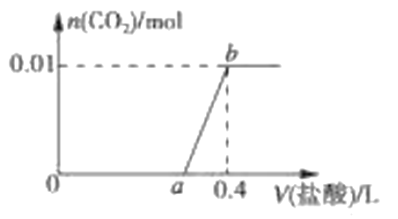
A. 在0a范围内,只发生NaOH和HCl的反应
B. ab段发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的化学方程式或离子方程式中不正确的是
A. 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH—=SiO32—+H2O
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2H++2I—+H2O2=I2+2H2O
C. 燃煤时加入适量石灰石粉末,可减少SO2的排放:2CaCO3+2SO2+O2![]() 2CaSO4+2CO2
2CaSO4+2CO2
D. 强碱溶液中,用次氯酸钠与Fe(OH)2反应制备高铁酸钠:2ClO—+ Fe(OH)2=FeO42—+2Cl—+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芦笋中的天冬酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,________(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有________种。
(3)H2S和H2Se的参数对比见下表。
化学式 | 键长/nm | 键角 | 沸点/℃ |
H2S | 1.34 | 92.3° | -60.75 |
H2Se | 1.47 | 91.0° | -41.50 |
①H2Se分子中含有的共价键类型为_____________(填“σ”或“π”)。
②H2S的键角大于H2Se的原因可能为______________________________。
③H2Se的酸性比H2S________(填“强”或“弱”)。
(4)已知钼(Mo)位于第五周期ⅥB族,钼、铬、锰的部分电离能如下表所示:
编号 | I5/kJ·mol-1 | I6/kJ·mol-1 | I7/kJ·mol-1 | I8/kJ·mol-1 |
A | 6990 | 9220 | 11500 | 18770 |
B | 6702 | 8745 | 15455 | 17820 |
C | 5257 | 6641 | 12125 | 13860 |
A是____________(填元素符号),B的价电子排布式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
A | 原子核外有6种不同运动状态的电子 |
C | 基态原子中s电子总数与p电子总数相等 |
D | 原子半径在同周期元素中最大 |
E | 基态原子最外层电子排布式为3s23p1 |
F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素位于元素周期表第_______周期_______族;C元素和F元素的电负性比较,较小的是________。
(2)D的单质在空气中燃烧时火焰的颜色是__________________,请用原子结构的知识解释发光的原因:__________________________。
(3)H元素位于元素周期表的_________区。基态E原子的L层电子排布图为__________。
(4)B元素与宇宙中含量最丰富的元素形成的最简单化合物的VSEPR模型为________,B元素与同周期相邻两元素的电离能大小关系为______________ , 请解释原因__________________________________。
(5)G元素的低价阳离子的离子结构示意图是________,F元素原子的价电子的电子排布图是________。
(6)在基态G中,电子占据的最高能层符号为________,该能层具有的原子轨道数为____________。
(7)G的高价阳离子的溶液与H单质反应的离子方程式为___________________________;
(8)与E元素成对角线关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求表达下列变化过程中的化学用语,其中⑴~⑶写化学方程式,⑷~⑸写离子方程式。
(1)金属镁在CO2中燃烧__________________________________________
(2)加热碳酸氢钠固体____________________________________________
(3)二氧化硫与氢氧化钠溶液反应__________________________________
(4)KCl溶液与AgNO3溶液反应_____________________________________
(5)铜与稀硝酸反应制取NO气体____________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com