
| A. | 单质的氧化性:X<M | |
| B. | 气态氢化物的热稳定性:M>N | |
| C. | X与Y简单离子半径:r(X离子)<r(Y离子) | |
| D. | 化合物ZX2与ZN4含有相同类型的化学键 |
分析 X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,已知X的最外层电子数是次外层电子数的3倍,则X是O元素;
X、M同主族,且M的原子序数大于X,所以M是S元素;
Y在同周期主族元素中原子半径最大,且原子序数大于X的短周期元素,则Y是Na元素;
Z的最高化合价与最低化合价的代数和为零,且原子序数大于Y,所以Z是Si元素;
N是原子序数大于M的短周期主族元素,所以N是Cl元素,以此解答该题.
解答 解:X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增,已知X的最外层电子数是次外层电子数的3倍,则X是O元素;
X、M同主族,且M的原子序数大于X,所以M是S元素;
Y在同周期主族元素中原子半径最大,且原子序数大于X的短周期元素,则Y是Na元素;
Z的最高化合价与最低化合价的代数和为零,且原子序数大于Y,所以Z是Si元素;
N是原子序数大于M的短周期主族元素,所以N是Cl元素,
A.同一主族元素中,随着原子序数的增大元素的非金属性逐渐减弱,其单质的氧化性逐渐减弱,故A正确;
B.同一周期非金属元素中,氢化物的稳定性随着原子序数的增大而增大,故B错误;
C.电子层数相同的阴阳离子,阴离子半径大于阳离子半径,所以r(X离子)>r(Y离子),故C错误;
D.化合物SiO2与SiCl4都是共价化合物,都只含共价键,所以含有相同类型的化学键,故D正确;
故选AD.
点评 本题以元素推断为载体考查元素化合物、元素周期律知识,正确推断元素的解本题关键,明确电子层结构相同离子半径的比较方法,为常考查点.


科目:高中化学 来源: 题型:选择题
| A. | Al | B. | Na | C. | Cu | D. | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它属于新型无机非金属材料 | |
| B. | 补血口服液中添加维生素C,作为氧化剂 | |
| C. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 | |
| D. | 国务院要求坚决控制钢铁、水泥、焦炭等行业落后产能总量,是落实“低碳经济”的具体举措 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3 | B. | NO2 | ||
| C. | HCl | D. | 体积比为4:1的NO2和O2的混合气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+和Al(OH)3 | B. | Al(OH)3 | C. | AlO2- | D. | AlO2-和Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
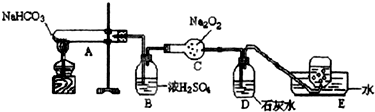
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O和Na2O2都能与水反应生成NaOH,所以他们是碱性氧化物 | |
| B. | 向饱和Na2CO3溶液中通入足量CO2,反应的离子方程式为CO32-+CO2+H2O═2HCO32- | |
| C. | NaCl可作为工业冶炼钠的原料,冶炼应在无水条件下进行 | |
| D. | 固体NaOH的潮解和Na2CO3•10H2O的风化均为物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 以Al作阳极,Fe作阴极,可以实现铁上镀铝 | |
| B. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解 | |
| C. | 向纯水中加入盐酸或降温,都能使水的电离平衡逆向移动,水的离子积减小 | |
| D. | 3C(s)+CaO(s)═CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com