
 �ö������ȣ�ClO2�����������ƣ�Na2FeO4Ħ������Ϊ166g•mol-1�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+��
�ö������ȣ�ClO2�����������ƣ�Na2FeO4Ħ������Ϊ166g•mol-1�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+������ ��1���Ե�λ���������������õ��ĵ���������ʾ����Ч�ʣ���������Ϊm������Ч�ʷֱ�Ϊ$\frac{m}{67.5}$��5��$\frac{m}{166}$��3��$\frac{m}{71}$��2��1��
��2����A�з�Ӧ������K2CO3��ClO2��CO2����Ϸ�Ӧ������������д��Ӧ����ʽ��
��BΪClO2������װ�ã���ˮ��ȴ��
��C��Ϊ�ܷ�װ�ã��������岻���ų���
��ClO2��NaOH��Ӧ��Ӧʱ���������ƺ��������ƣ�NaClO2�������m=cVM���㣮
��� �⣺��1���Ե�λ���������������õ��ĵ���������ʾ����Ч�ʣ���������Ϊm������Ч�ʷֱ�Ϊ$\frac{m}{67.5}$��5��$\frac{m}{166}$��3��$\frac{m}{71}$��2��1�������ɴ�С��˳��ΪClO2��Cl2��Na2FeO4���ʴ�Ϊ��Na2FeO4��Cl2��ClO2��
��2����A�з�Ӧ������K2CO3��ClO2��CO2���ɷ�Ӧ�����������֪��ӦΪ2KClO3+H2C2O4=K2CO3+ClO2��+CO2��+H2O��
�ʴ�Ϊ��2KClO3+H2C2O4=K2CO3+ClO2��+CO2��+H2O��
��B���ֻ�Ӧ����װ��Ϊ��ˮԡ����װ�û�ʢ�б�ˮ��ˮ�ۣ��ʴ�Ϊ����ˮԡ����װ�û�ʢ�б�ˮ��ˮ�ۣ�
��C��Ϊ�ܷ�װ�ã��������岻���ų����ɵ�������ը�ѣ���C���������ʴ�Ϊ��C��
��ClO2��NaOH��Ӧ��Ӧʱ���������ƺ��������ƣ�NaClO2�������ӷ�ӦΪ2ClO2+2OH-�TClO3-+ClO2-+H2O����Ҫ450mL 0.4mol/L��NaOH��Һ�����ھ�ȷ����ʱ����Ҫ����ȡNaOH������0.5L��0.4mol/L��40g/mol=8.0g���ʴ�Ϊ��2ClO2+2OH-�TClO3-+ClO2-+H2O��8.0��
���� ���⿼��������ԭ��Ӧ�ļ��㼰����ʵ�鷽������ƣ�Ϊ��Ƶ���㣬����������ԭ��Ӧ��Ԫ�صĻ��ϼ۱仯��ʵ����Ƽ�ʵ��װ�õ����õ�Ϊ���Ĺؼ������ط��������㼰ʵ���������ۺϿ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʯȼ�ϵ�ȼ�����������������һ����Ҫ���� | |
| B�� | ���ؽ������ӵĵ��Һ���������ŷ� | |
| C�� | ú����������Һ�����������仯���̺��Ϊ�����Դ������ú���ۺ����õķ��� | |
| D�� | �Ľ�����β���������������ٴ�����Ⱦ����ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ƚ�Cu��Fe�Ļ�ԭ�ԣ�ͭ������������Һ�� | |
| B�� | �Ƚ�þ�����Ľ����ԣ�ȡһС��ȥ����Ĥ��þ������Ƭ���ֱ����1.0 mol•L-1�������� | |
| C�� | �Ƚϸ�����ء������������ԣ���������м���Ũ���� | |
| D�� | �Ƚ��ȡ���ķǽ����ԣ��廯����Һ��ͨ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ����
���� ��
�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢܢݢ� | B�� | �٢ڢۢݢ� | C�� | �ڢۢݢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ֱ���H2O2��KMnO4�ֽ���O2�����Ƶõ�����O2ʱ��ת�Ƶ�����֮��Ϊ1��1 | |
| B�� | �����£�0.1 mol•L-1 NH4NO3��Һ�к��еĵ�ԭ������0.2NA | |
| C�� | ���³�ѹ�£�3.2 g O2��3.2 g O3������ԭ��������0.2NA | |
| D�� | 1mol ������������ԼΪ10NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L��ˮ����NA��Cl2���� | |
| B�� | ��1 L 0.1 mol•L-1̼������Һ����������������0.1NA | |
| C�� | 50 mL18.4 mol•L-1Ũ����������ͭ�ȷ�Ӧ������SO2������ĿΪ0.46NA | |
| D�� | ��״���£���H2O2�Ƶ�4.48 LO2ת�Ƶĵ�����ĿΪ0.8NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� | 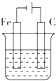 | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ṹ����֪����Ӧ�������ᣨѡ�������ǿ������
������ṹ����֪����Ӧ�������ᣨѡ�������ǿ�������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com