
| A. | 在小苏打溶液中:NO3-、AlO2-、NH4+、K+ | |
| B. | 在空气中:H2S、CO2、SO2、CO | |
| C. | 在酸性高锰酸钾溶液中:C2H5OH、Na+、SO42-、CO32- | |
| D. | 在pH=8的溶液中:Na+、HCO3-、Br-、Mg2+ |
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
有一处于平衡状态的反应:X(s)+3Y(g)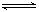 2Z(g)ΔH<0。为了使平衡向生成Z 的方向移动,应选择的条件是( )
2Z(g)ΔH<0。为了使平衡向生成Z 的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加正催化剂 ⑥分离出Z
A.①③⑤ B.②③⑥ C.②③⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省唐山市高二上10月月考化学试卷 (解析版) 题型:选择题
已知1 g H2完全燃烧生成水蒸气放出热量121 kJ,且O2中1 mol O===O键完全断裂时吸收热量496 kJ,水蒸气中形成1 mol H—O键时放出热量463 kJ,则H2中1 mol H—H键断裂时吸收的热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
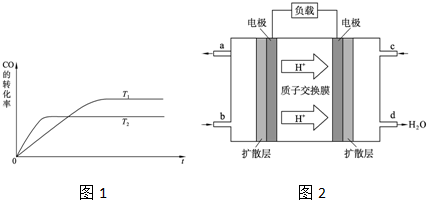
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化学反应过程中,发生物质变化的同时不一定发生能量变化 | |
| B. | 需要加热才能发生的化学反应,它可能是吸热反应也可能是放热反应 | |
| C. | 反应产物的总焓大于反应物的总焓时,反应吸热,△H<0 | |
| D. | △H的大小与热化学方程式的计量系数无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | B. | 石墨和金刚石是同一种物质 | ||
| C. | 氯化铵、蔗糖都属于电解质 | D. | 碘单质和碘蒸气互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
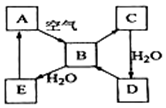 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
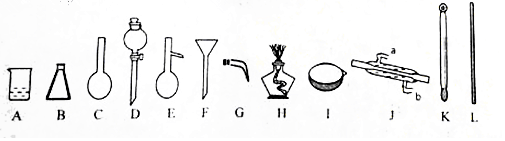
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
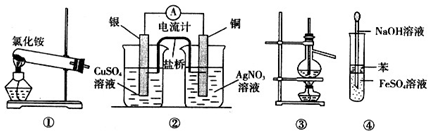
| A. | 实验室用装置①制取氨气 | |
| B. | 装置②将化学能转化为电能 | |
| C. | 装置③可用于分离沸点相差较大的互溶液体混合物 | |
| D. | 装置④可用于 Fe(OH)2的制取,并能防止 Fe(OH)2被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com