
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年湖北荆州中学高一上学期期中考试化学试卷(解析版) 题型:推断题
已知反应:2H2CrO4 + 3H2O2=2Cr(OH)3 + 3O2↑+ 2H2O,该反应中H2O2只发生如下变化过程:H2O2→O2
(1)该反应中的还原剂是 。
(2)用单线桥法表示反应中电子转 移的方向和数目:2H2CrO4 + 3H2O2=2Cr(OH)3 + 3O2↑+ 2H2O。
移的方向和数目:2H2CrO4 + 3H2O2=2Cr(OH)3 + 3O2↑+ 2H2O。
(3)如反应中转移了0.6mol 电子,则
电子,则 产生的气体在标准状况下体积为
产生的气体在标准状况下体积为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建厦门一中高一上期中考试化学试卷(解析版) 题型:选择题
不能实现下列物质间直接转化的元素是:
单质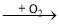 氧化物
氧化物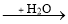 酸或碱
酸或碱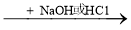 盐
盐
A.碳 B.钠 C.硫 D.铁
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京顺义牛栏山一中高一上期中化学试卷(解析版) 题型:实验题
海洋植物如海带.海藻中含有丰富的碘元素,其主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:(已知: 2I—+ Cl2=2Cl—+I2)
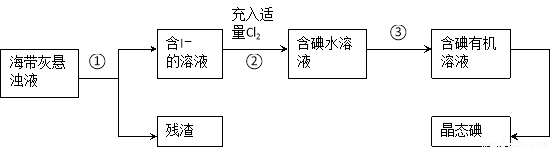
(1) 指出提取碘的过程中有关的实验操作名称:① ,③ ;
(2) 过程②中充入适量Cl2的目的是 ;
(3) i)操作③中所用的有机试剂可以是 (填代号)
A.乙醇(与水互溶) B.四氯化碳 C.甲烷气体 D.食盐水
ii)简述要把碘水变成碘有机溶液对于提取晶体碘的优点 。
(4) 操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50ml碘水和15ml有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. ;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(a) 过程③的操作顺序是 C、 B、 D、 A、 H、 G、 E、 F,则E的操作步骤是 ;
(b) 上述G步操作的目的是: ;
(c) 最后碘的有机溶液是通过 获得(填“漏斗上口”或“漏斗下口”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京顺义牛栏山一中高一上期中化学试卷(解析版) 题型:选择题
等质量的SO2和SO3 ,下列说法正确的是
A.所含氧原子的个数比为2∶3 B.所含硫原子的个数比为1∶1
C.所含氧元素的质量比为6∶5 D.所含硫元素的质量比为5∶4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽合肥第一六八中学高一上期中化学试卷(解析版) 题型:选择题
赤铜矿的主要成分是氧化亚铜(Cu2O),辉铜矿的主要成分是硫化亚铜(Cu2S),将赤铜矿与辉铜矿混合加热有如下反应:Cu2S+2Cu2O=6Cu+SO2↑,下列对于该反应的说法正确的是
A.该反应中的氧化剂只有Cu2O
B.Cu既是氧化产物又是还原产物
C.Cu2S在反应中既是氧化剂又是还原剂
D.氧化产物与还原产物的物质的量之比为6:1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:填空题
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
(1)反应的△H 0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。
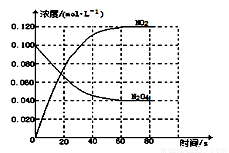
在0~60s时段,反应速率v(N2O4)为 mol?L-1?s-1,
平衡时混合气体中NO2的体积分数为 。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol?L-1?s-1的平均速率降低,经10s又达到平衡。
①T 100℃(填“大于”“小于”),
②列式计算温度T时反应的平衡常数K 。
(3)温度T时反应达平衡后,向容器中,迅速充入含0.08mol的NO2和0.08mol N2O4 的混合气体,此时速率关系v(正) v(逆)。(填“大于”,“等于”,或“小于”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:填空题
资料一:考古工作者从安阳的商代铸铜遗址中,发现当时冶炼铜的主要矿物原料是孔雀石(Cu2(OH)2CO3),主要燃料是木炭,冶炼温度估计在1000 ℃左右。
资料二:西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”。“曾青”可能是硫酸铜一类的物质,将孔雀石溶于硫酸中得此溶液,当把铁粉投入此溶液中即可得铜。
(1)关于“曾青”和孔雀石的水溶性分析中,判断正确的是( )
A.前者可溶,后者难溶 B.前者难溶,后者可溶
C.两者均可溶 D.两者均难溶
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有( )
①Cu2(OH)2CO3 2CuO+CO2↑+H2O ②2CuO+C
2CuO+CO2↑+H2O ②2CuO+C  2Cu+CO2↑
2Cu+CO2↑
③CuO+CO Cu+CO2 ④CO2+C
Cu+CO2 ④CO2+C 2CO
2CO
A.①② B.①③ C.①②③ D.①②③④
(3)在(2)的四个反应中,不属于四种基本反应类型的有(填序号,下同)_________,不属于氧化还原反应的有___________。
(4)资料二中,假设溶解孔雀石的酸是稀硫酸,写出用此方法冶炼铜的化学方程式 , 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都七中高二上12月月考化学试卷(解析版) 题型:选择题
对某酸性溶液(可能含有Br-、SO42-、H2SO3、NH4+等微粒)。分别进行如下实验:(1)加热,放出的气体可以使品红溶液褪色;(2)取原溶液加碱,调至溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝;(3)取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。对于下列微粒不能确认其在原溶液中是否存在的是( )
A.Br- B.SO42- C.H2SO3 D.NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com