
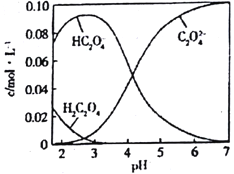
【题目】H2C2O4为二元弱酸。20℃时,有一组H2C2O4和NaOH的混合溶液,其中c (H2C2O4) +c (HC2O4)+c (C2O42-)=0.1mol/L,溶液中部分微粒的物质的量浓度随pH 的变化如图所示。[电离度=( 已电离电解质分子数/原弱电解质分子数) x 100%] 下列说法不正确的是
A. H2C2O4的Ka2数量级为10-5
B. 在NaHC2O4溶液中,c (Na+)>c(HC2O4)>c (H+)>c(C2O42-)>c (OH-)
C. 0.1mol/L 的H2C2O4溶液,H2C2O4的电离度约为80%
D. pH=7.0的溶液中,c (Na+)=0.1+c(C2O42-)-c (H2C2O4)
【答案】C
【解析】A、Ka2= ,电离平衡常数只受温度的影响,c(C2O42-)=c(HC2O4-)时,Ka2=c(H+),根据图像,H2C2O4的Ka2数量级为10-5,故A说法正确;B、根据图像,NaHC2O4的溶液显酸性,即HC2O4-的电离程度大于其水解程度,因此离子浓度大小顺序是c (Na+)>c(HC2O4-)>c (H+)>c(C2O42-)>c (OH-),故B说法正确;C、H2C2O4
,电离平衡常数只受温度的影响,c(C2O42-)=c(HC2O4-)时,Ka2=c(H+),根据图像,H2C2O4的Ka2数量级为10-5,故A说法正确;B、根据图像,NaHC2O4的溶液显酸性,即HC2O4-的电离程度大于其水解程度,因此离子浓度大小顺序是c (Na+)>c(HC2O4-)>c (H+)>c(C2O42-)>c (OH-),故B说法正确;C、H2C2O4![]() HC2O4-+H+,根据电离度的定义,已电离的H2C2O4的浓度等于生成的HC2O4-的浓度,根据图像,开始时c(C2O42-)约为0.072mol·L-1,草酸的电离度为0.072/0.1×100%=72%<80%,故C说法错误;D、根据电荷守恒,则有c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),c (H2C2O4) +c (HC2O4)+c (C2O42-)=0.1mol/L,pH=7,即c(H+)=c(OH-),因此有,c (Na+)=0.1+c(C2O42-)-c (H2C2O4),故D说法正确。
HC2O4-+H+,根据电离度的定义,已电离的H2C2O4的浓度等于生成的HC2O4-的浓度,根据图像,开始时c(C2O42-)约为0.072mol·L-1,草酸的电离度为0.072/0.1×100%=72%<80%,故C说法错误;D、根据电荷守恒,则有c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-),c (H2C2O4) +c (HC2O4)+c (C2O42-)=0.1mol/L,pH=7,即c(H+)=c(OH-),因此有,c (Na+)=0.1+c(C2O42-)-c (H2C2O4),故D说法正确。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是:
A. 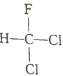 和
和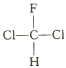 互为同分异构体
互为同分异构体
B. 15g甲基(﹣CH3)含有的电子数是9NA
C. 7.8g苯中含有的碳碳双键数为0.3NA
D. 标准状况下,2.24 L CCl4中的原子总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以食盐为原料进行生产并综合利用的某些过程如图。
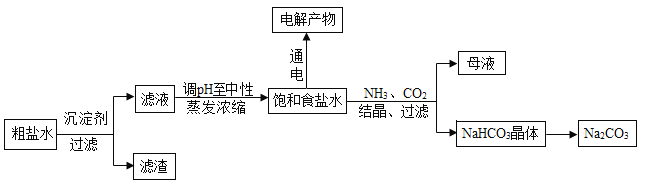
(1) 除去粗盐中的微溶物质CaSO4通常用Na2CO3处理,请用平衡移动原理解释说明:_____________。
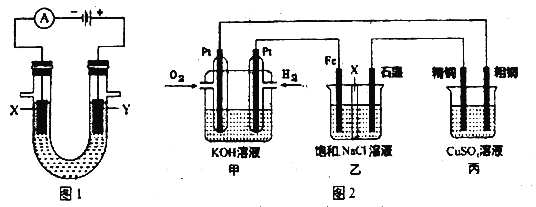
(2) 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.图1表示电解饱和NaCl 溶液的装置,X、Y是石墨棒。实验开始后,检验Y 电极反应产物的方法是_________________。
(3) 若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是__________。
(4) 某同学设计一个燃料电池(如图2所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。根据要求回答相关问题:
①通入氢气电极的反应式为__________________。
②反应一段时间后,在乙装置中滴入酚酞溶液,______________(填“铁”或“石墨”)极区的溶液先变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将___________(填“增大”“减小”或“不变”)。
④若在标准状况下有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )
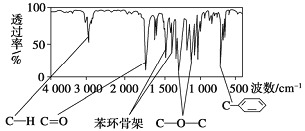

A. 与A属于同类化合物的同分异构体只有2种
B. A在一定条件下可与4molH2发生加成反应
C. A分子属于酯类化合物,在一定条件下不能发生水解反应
D. 符合题中A分子结构特征的有机物只有1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 1mol 的P4O6中含有6 NA个P—O键
B. 0.1mo1H2和0.1molI2于密闭容器中充分反应后,分子总数小于0.2 NA
C. pH=3的CH3COOH溶液中,含有10-3NA个H+
D. 高温下,16.8gFe 与足量的水蒸气反应,失去0.8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请在标有序号的空白处填空:以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答有关问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)__________。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl→CH3CH2Cl+H2O
C.CH3CH3+Cl2![]() CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2![]() CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性高的是__________反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式________,并说明该方法的优点_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是

A. b极发生氧化反应
B. a极的反应式:N2H4+4OH--4e-=N2↑+4H2O
C. 放电时,电流从a极经过负载流向b极
D. 其中的离子交换膜需选用阳离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com