
| A. | 丁达尔效应可用于鉴别胶体和溶液 | |
| B. | 胶体粒子的直径在1~100 nm之间 | |
| C. | 胶体一定是混合物 | |
| D. | 将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体 |
科目:高中化学 来源: 题型:实验题
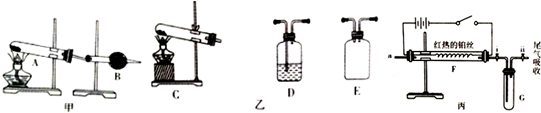
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在一定条件下,能发生取代、氧化、水解、酯化和加聚反应 | |
| B. | 该物质分子中最多可以有9个碳原子在同一平面上 | |
| C. | 1 mol该物质最多可与5mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
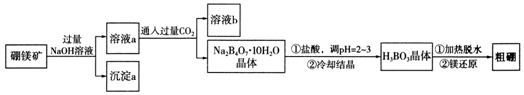

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水是一种很好的溶剂 | B. | 水在人体内还有调节体温的作用 | ||
| C. | 饮用水越纯净对身体越好 | D. | 水是反应介质和反应物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,将22.4 L HC1溶于1L水,可配成1 mol•L-l的稀盐酸 | |
| B. | 将100 mL 18 mol•L-1的浓H2SO4和100 mL水混合,可配成9 moI•L-l的H2SO4溶液 | |
| C. | 将4.0 g NaOH溶于100 mL容量瓶中,加水至刻度线,配成1 mol•L-1的NaOH溶液 | |
| D. | 将0.1 mol NaCl配成100 mL溶液,从中取出10 mL,所取出溶液的物质的量浓度为1 mol•L-l |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,溶液中的铝离子向正极移动 | |
| B. | 该电池可能是一种可充电的二次电池 | |
| C. | 消耗相同质量金属时,用锂做负极时,产生电子的物质的量比铝多 | |
| D. | 该电池负极的电极反应为:Al-3e-═Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com