
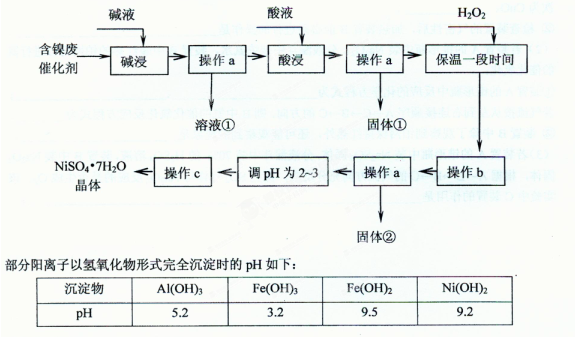
 2H++ Fe(OH)2在25℃时的平衡常数
2H++ Fe(OH)2在25℃时的平衡常数 


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:不详 题型:单选题
| A.将烧杯中的浓氨水加热 |
| B.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中 |
| C.在烧瓶中将氢氧化钠浓溶液和氯化铵溶液混合加热 |
| D.直接加热试管中的氯化铵固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 8分,每空2分)
8分,每空2分)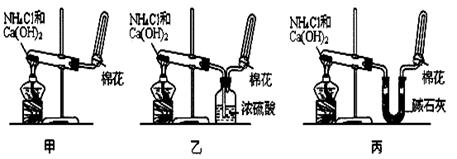
 上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是___填(“甲”、“乙”或“丙”)。
上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是___填(“甲”、“乙”或“丙”)。
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
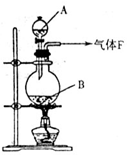
 离子方程式为______________________________________________;
离子方程式为______________________________________________; 足量的MnO2反应制Cl2,结果制得的Cl2体积(标准状况下)小于1.12L,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:___________________________________________________。
足量的MnO2反应制Cl2,结果制得的Cl2体积(标准状况下)小于1.12L,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:___________________________________________________。
 物质的量为____________________。
物质的量为____________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
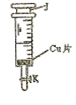
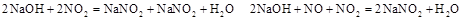
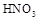 中,吸取适量的
中,吸取适量的 稀
稀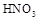 ,然后迅速关闭阀门K,请回答此时可能观察到的实验现象: 。
,然后迅速关闭阀门K,请回答此时可能观察到的实验现象: 。 ,当注射器活塞上升到某一位置时,迅速打开阀门K,将反应液推入NaOH溶液中后关闭K。
,当注射器活塞上升到某一位置时,迅速打开阀门K,将反应液推入NaOH溶液中后关闭K。 学方程式并配以必要的文字说明)。
学方程式并配以必要的文字说明)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
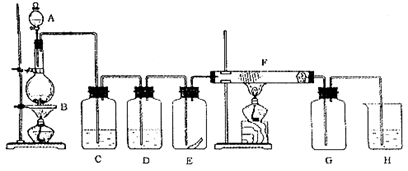
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
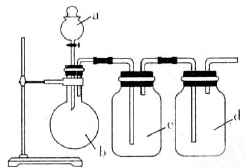
| 选项 | 制取气体 | a | b | c | d |
| A | NO | 稀硝酸 | 铜片 | H2O | 浓硫酸 |
| B | O2 | 双氧水 | MnO2 | H2O | 浓硫酸 |
| C | NH3 | 浓氨水 | 碱石灰 | 浓硫酸 | H2O |
| D | SO2 | 浓盐酸 | Na2SO3粉末 | NaHSO3溶液 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com