
为了预防碘缺乏症,国家规定每千克食盐中应含有40~50 mg碘酸钾。碘酸钾晶体具有较高的稳定性,但在酸性溶液中,碘酸钾是一种较强的氧化剂,能跟某些还原剂反应生成碘;在碱性溶液中,碘酸钾能被氯气、次氯酸等更强的氧化剂氧化为更高价的碘的含氧酸盐。工业生产碘酸钾的流程如图所示。
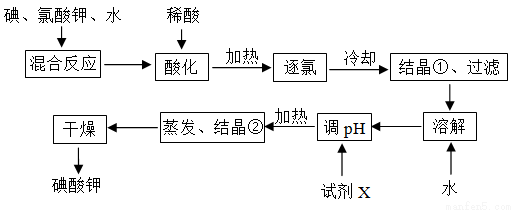
(1)碘在周期表中的位置为__________________;
(2)碘、氯酸钾、水混合反应时,若两种还原产物所得电子的数目相同,请配平该反应的化学方程式:____I2+____KClO3+____H2O=____KH(IO3)2+____KCl+____Cl2↑;
(3)混合反应后,用稀酸酸化的作用是___________________________,在稀盐酸和稀硝酸中不能选用的酸是_________,理由是__________________________________;
(4)试剂X的化学式为__________,写出用试剂X调pH的化学方程式__________________;
(5)如果省略“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂X调整反应混合物的pH,对生产碘酸钾有什么影响?________________________________________。
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:2016届辽宁师大附中高三下学期精品考试理综化学试卷(解析版) 题型:推断题
某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下,转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为(C7H5NO)。

已知: (苯胺,易被氧化)
(苯胺,易被氧化)
(1) X的名称是 ,反应①②③④⑤中属于氧化反应的是 。
(2)反应②③两步能否互换 (填“能”或“不能”),理由是 。
(3)反应④的化学方程式是 。
(4) 的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件: ①芳香族化合物, ②能发生水解反应, ③与FeCl3溶液能够发生显色反应;
的同系物M比其本身相对分子质量大14,M的同分异构体中能同时满足以下条件: ①芳香族化合物, ②能发生水解反应, ③与FeCl3溶液能够发生显色反应;
共有 (不考虑立体异构)种。
(5)请用合成反应流程图表示出由 和其他无机物合成
和其他无机物合成 最合理的方案。 。
最合理的方案。 。
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:简答题
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) 平衡常数为 K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g) 平衡常数为 K1;反应②Fe(s)+H2O(g) FeO(s)+H 2 (g) 平衡常数为 K2;
FeO(s)+H 2 (g) 平衡常数为 K2;
测得在不同温度下, K1、K2值如下:

(1)在500℃时进行反应①,若CO2起始浓度为1mol·L -1,10分钟后达到平衡,则V(CO)为______。
(2)在 900℃时反应 CO2 (g)+H2(g) CO(g)+H2O(g)的平衡常数 K=___________。
CO(g)+H2O(g)的平衡常数 K=___________。
(3)700℃反应②达到平衡,其它条件不变时,使得该平衡向右移动,可以采取的措施有______(选填编号)。
A.缩小反应器体积 B.加入水蒸气
C.降低温度到500℃ D.加入Fe粉
(4)如果上述反应①在体积不变的密闭容器中发生,能说明反应已达到平衡状态的是________(选填编号)。
A.v正(CO)= v 逆 (CO2) B.C(CO) = C(CO2)
C.容器内气体的密度不变 D.容器内压强不变
(5)若反应①在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件再达平衡后,相应物质的物理量如何变化?(选填“增大”、“减小”或“不变”)
①降低温度,CO2的平衡浓度______________;
②再通入CO2,CO2的转化率_________________。
(6)下列图像符合反应①的是__________(填序号)(图中 v 是速率、φ 为混合其中CO含量,T为温度)

查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下冲刺模拟理综化学C卷(解析版) 题型:填空题
黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S═K2S+N2↑+3CO2↑(已配平)
(1)除S外,上列元素的第一电离能从大到小依次为___________________________;
(2)生成物中,A 的电子式为____________;含极性共价键的分子的中心原子轨道杂化类型_____________;
(3)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(4)S的基态原子价层电子排布式为___________,S的一种化合物ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0pm,密度为________g·cm3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________pm。

查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下冲刺模拟理综化学C卷(解析版) 题型:选择题
短周期X、Y、Z、W四种元素在元素周期表中位置如图所示。有关表述正确的是( )
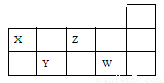
A. X、Y、W的最高价氧化物对应水化物均属强酸
B. Y的氢化物能与Y的最高价氧化物对应水化物反应
C. 原子半径从大到小依次为X>Z>Y>W
D. Z的氢化物的沸点低于W的氢化物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二6月月考化学试卷(解析版) 题型:选择题
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol·L-1 的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A.开始加入合金的质量可能为16.4g
B.标准状况下产物NO的体积为22.4L
C.生成沉淀完全时消耗NaOH溶液的体积为100mL
D.参加反应的硝酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二6月月考化学试卷(解析版) 题型:选择题
已知高炉炼铁的化学方程式为Fe2O3+3CO 2Fe+3CO2。下列对该反应的叙述不正确的是
2Fe+3CO2。下列对该反应的叙述不正确的是
A.CO是还原剂 B.Fe2O3被还原
C.氧化产物是CO2 D.属于置换反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁沈阳二中高一6月月考化学试卷(解析版) 题型:选择题
某实验小组依据反应AsO43-+2I-+2H+ AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
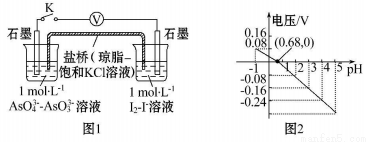
A.调节pH可以改变反应的方向
B.pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁师大附中高一下学期6月月考化学试卷(解析版) 题型:选择题
在气相条件下(T=500 K),有相同体积的甲、乙两容器,甲容器充人1 g SO2、l gO2,乙容器充人2 g SO2、2g O2则下列叙述中正确的是
A.化学反应速率:乙>甲 B.平衡后SO2的浓度:乙<甲
C.SO2转化率:乙<甲 D.平衡后O2的体积分数:乙>甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com