
| A. | 催化剂是影响化学反应速率的主要因素 | |
| B. | 化学反应的反应热与反应途径无关 | |
| C. | 增大压强一定能增大化学反应速率 | |
| D. | 反应物分子间发生碰撞即可发生化学反应 |
分析 A、影响化学反应速率的主要因素是反应物本身性质;
B、根据盖斯定律解答;
C、对于气相反应,增大压强化学反应速率会加快;
D、反应物分子的每次碰撞不一定都能发生化学反应.
解答 解:A、影响化学反应速率的主要因素是反应物本身性质,而催化剂是外界条件,故A错误;
B、根据盖斯定律可知,反应热只与反应体系的始态和终态有关,而与反应的途径无关,故B正确;
C、只有对于气相反应,增大压强化学反应速率会加快,没有气体参与的反应,压强对化学反应速率无影响,故C错误;
D、反应物分子的每次碰撞不一定能发生化学反应,只有活化分子的有效碰撞才能发生化学反应,故D错误;
故选B.
点评 影响化学反应速率的因素:温度、浓度、压强、催化剂,注意各个因素的使用条件是关键,难度不大.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 2:71 | B. | 71:2 | C. | 1:8 | D. | 8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | DMC的结构简式为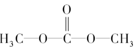 | |
| B. | DMC在空气不能燃烧 | |
| C. | DMC易溶于水,不溶于乙醇和丙酮 | |
| D. | DMC用于生产非毒性化工产品,故被誉为有机合成的“绿色化工原料” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4 L CO2中含有NA个CO2分子 | |
| B. | 1.7 g H2O2中含有的电子数为0.9NA | |
| C. | 标准状况下,2.24 L乙醇含有的分子数等于0.1NA | |
| D. | 分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
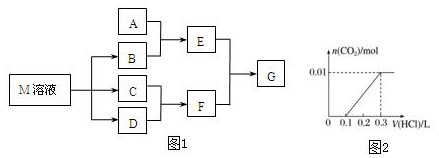

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④ | C. | ②⑤⑥ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 制备方法 | 化学共沉淀法 | 碾磨法 | 蒸着(zhuó)法 |
| 制得磁流体颗粒直径 | 大约40纳米左右 | 大于300纳米 | 2-10纳米 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、Al3+、Na+、SO42- | B. | I-、NO3-、K+、NH4+ | ||
| C. | MnO4-、Cl-、SO42-、K+ | D. | SiO32-、SO32-、Na+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com