
【题目】常温下,两种溶液① 0.1 mol/L NH3·H2O ② 0.1 mol/L NH4Cl 中:
(1)溶液①的 pH_______7(填“>”、“<”或“=”),其原因是_________(用离子方程式表示)。
(2)溶液②呈_______性(填“酸”、“碱”或“中”)。水解反应是吸热反应,升温可以_______(填“促进”或“抑制”)NH4Cl 的水解。
(3)两种溶液中 c(![]() ) 的大小为_____(填字母)。
) 的大小为_____(填字母)。
a.两种溶液中 c(![]() ) 都等于 0.1 mol/L
) 都等于 0.1 mol/L
b.两种溶液中 c(![]() ) 都小于 0.1 mol/L
) 都小于 0.1 mol/L
c.NH4Cl 溶液中 c(![]() ) 小于 NH3·H2O 溶液中 c(
) 小于 NH3·H2O 溶液中 c(![]() )
)
【答案】> NH3·H2O![]() NH4++OH- 酸 促进 b
NH4++OH- 酸 促进 b
【解析】
(1)NH3·H2O是弱碱,在水溶液能电离出氢氧根离子:NH3·H2O![]() NH4++OH-,导致溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,溶液的pH>7;
NH4++OH-,导致溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,溶液的pH>7;
(2)氯化铵是强酸弱碱盐,铵根离子能水解导致溶液中氢离子浓度大于氢氧根离子浓度,溶液呈酸性;盐类水解反应是吸热反应,升高温度平衡向正反应方向移动,所以能促进水解;
(3)氨水是弱电解质,在水中电离程度很小,铵根离子浓度很小;氯化铵是强酸弱碱盐,能水解但水解程度很小,主要以电离为主,所以相同浓度的氨水和氯化铵溶液,氯化铵溶液中铵根离子浓度较大,但都小于0.1mol/L,故选b。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应2HI(g)![]() H2(g)+ I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是: ①增大氢气的浓度 ②升高温度 ③降低温度 ④缩小体积 ⑤增大HI的浓度 ⑥减小压强
H2(g)+ I2(g)(正反应吸热)达到平衡时,要使混合气体的颜色加深,可采取的措施是: ①增大氢气的浓度 ②升高温度 ③降低温度 ④缩小体积 ⑤增大HI的浓度 ⑥减小压强
A. ①③⑥ B. ③⑤⑥ C. ①③⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:2A(g)+B(g)![]() 2C(g) ΔH=QkJ/mol。相关条件和数据见下表:
2C(g) ΔH=QkJ/mol。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
平衡时n(C)/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A.K1=K2<K3
B.升高温度能加快反应速率的原因是降低了反应的活化能
C.实验Ⅱ比实验Ⅰ达平衡所需时间小的可能原因是使用了催化剂
D.实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molC,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 则
则![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种广谱、高效的消毒剂,易溶于水,尤其在水处理等方面有广泛应用。以下是某校化学研究小组设计实验制取ClO2的工艺流程图。下列有关说法正确的是( )
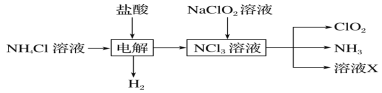
A.电解时发生反应的化学方程式为2HCl![]() Cl2↑+H2↑
Cl2↑+H2↑
B.由NaClO2溶液制取0.6 mol ClO2时,至少消耗0.1 mol NCl3
C.将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的 NH3
D.溶液X的成分为NaClO3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是将SO2 转化为重要的化工原料H2SO4的原理示意图。

请回答下列问题:
(1)该装置将________能转化为________能,电流方向为________(填“b→a”或“a→b”)。
(2)催化剂b表面O2发生___________反应,其附近酸性________(填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_________________________________________。
(4)若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两份质量均为mg的铝片分别置于盛有盐酸、NaOH溶液的两个烧杯中,待反应结束后,测得两个烧杯中溶液的质量均增加了![]() ,下列有关说法中错误的是
,下列有关说法中错误的是
A.![]()
B.两个烧杯中发生的反应所转移的电子数均为0.3NA
C.两个烧杯中消耗的溶质的物质的量之比为![]()
D.两个烧杯中生成的氢气的体积均为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂化和裂解过程得到的CH2=CH2,在一定条件下可以聚合成高分子化合物。含有 结构的化合物与CH2=CH2一样,可以在一定条件下聚合成高分子化合物。
结构的化合物与CH2=CH2一样,可以在一定条件下聚合成高分子化合物。
(1)广泛用作农用薄膜的聚氯乙烯塑料,是由CH2=CHCl在催化剂、加热的条件下聚合成的,其化学方程式是________________。
(2)电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯( ),它是由________________(写结构简式)聚合而成的。
),它是由________________(写结构简式)聚合而成的。
(3)CH2=CHCl与聚苯乙烯的单体在一定条件下可发生加聚反应,所得产物的结构简式为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com