
以苯酚为原料的合成路线如下所示,部分试剂和反应条件已略去。请按要求作答:
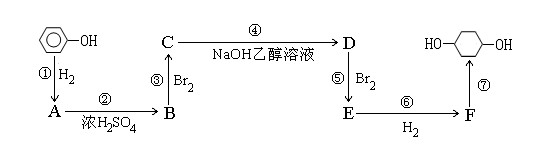
(1)写出以下物质的结构简式:
B: ; F: ;
(2)写出反应④⑤的化学反应方程式:
④
⑤
(3)在苯酚钠溶液中通入少量二氧化碳气体会出现浑浊,反应的离子方程式为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
铜是人类认识并应用最早的金属之一,我国是最早使用铜器的国家之一。铁与人类生活密切相关,几乎无处不在,是地壳中含量仅次于铝的金属。某研究性学习小组为了证明铁的金属活动性比铜强,设计了如下实验方案:
(1)将铁片置于硫酸铜溶液中有铜析出
(2)铁、铜和氯气反应分别生成FeCl3和CuCl2
(3)足量的铁粉和铜粉与浓硫酸在加热条件下反应分别生成FeSO4和CuSO4
(4)将铜片置于FeCl3溶液中铜片逐渐溶解
(5)把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生
(6)把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生
以上实验方案设计合理的有( )
A.两种 B.三种
C.四种 D.五种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )。
A.CH2Cl2有 两种结构
两种结构
B.烯烃跟氢气起加成反应产物是2,2,3,4-四甲基戊烷,则这样的烯烃有3种
C.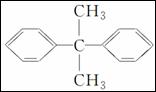 的一氯代物有5种
的一氯代物有5种
D.1 mol某烷烃完全燃烧消耗11 mol O2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.分子式为C9H10的含苯环的烯烃(不考虑立体异构)共有6种
B.芥子醇(  ) 能发生氧化、取代、水解、加聚反应
) 能发生氧化、取代、水解、加聚反应
C.实验室用乙醇制乙烯时,把生成的气体通入酸性KMnO4溶液,紫色褪去,不能说明一定生成了乙烯
D.将少量某物质的溶液滴加到新制银氨溶液中,水浴加热后有银镜生成,该物质不一定属于醛类
查看答案和解析>>
科目:高中化学 来源: 题型:
使用容量瓶配制溶液时,下列情况会使所配溶液浓度偏低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
A.①②③⑤ B.①②⑤ C.②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇汽油是由10%一25%的甲醇与其他化工原料、添加剂合成的新型车用燃料,可达到国标汽油的性能和指标。甲醇是一种可再生能源,具有广泛的开发和应用前景。
Ⅰ、工业上合成甲醇一般采用下列反应:CO(g)+2 H2(g) CH3 OH(g) △H=a kJ/mol,
CH3 OH(g) △H=a kJ/mol,
下表是该反应在不同温度下的化学平衡常数(K):
| 温度/0C | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
(1)由表中数据判断△H a 0(填“>”、“=”或“<”)。
(2)某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5 mol·L-1,则此时的温度为 0C。
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 浓度mol/L 时间/min | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
①反应从2 min到4 min之间,H2的反应速率为 。
②反应达到平衡时CO的转化率为 。
③反应在第2 min时改变了反应条件,改变的条件可能是 (填序号)。
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2 mol H2,发生反应CO(g)+2 H2(g)  CH3 OH(g)△H=a kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则
CH3 OH(g)△H=a kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则
w1 w2(填序号)。
A.大于 B.小于 C.等于 D.以上都有可能
Ⅱ、甲醇在化学电源方面也有着重要应 用。写出以甲醇为燃料,氢氧化钠溶液为电解质溶液的原电池中负极的电极反应式: 。
用。写出以甲醇为燃料,氢氧化钠溶液为电解质溶液的原电池中负极的电极反应式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com