
已知在相同状况下,同一化学键断裂需要吸收的能量等于形成该化学键放出的能量。下列说法错误的是( )
A.电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应
B.H2(g)+F2(g)=2HF(g) △H=-270 kJ/mol ,1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量
C.相同状况下,反应2SO2+O2=2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应
D.破坏1 mol氢气中的化学键消耗的能量为Q1 kJ,破坏1 mol氯气中的化学键消耗的能量为Q2 kJ,形成1 mol氯化氢中的化学键释放的能量为Q3 kJ,则Q1+Q2<2Q3
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省绍兴市一中高一上学期阶段性考试化学试卷(带解析) 题型:填空题
已知钠能与水剧烈反应:2Na+2H2O=2NaOH+H2↑
(1)相同质量的Na,Mg,Al与过量的盐酸反应,在相同的状况下,三者置换出的H2的体积比是____________________________。
(2)相同物质的量的Na,Mg,Al与过量的盐酸反应,在相同状况下,三者置换出的H2的体积比是_________________________。
(3)Na,Mg,Al与过量的盐酸反应,在相同状况下产生的氢气的体积相等,则Na,Mg,Al三种金属的物质的量之比是__________________________。
(4)将Na,Mg,Al各0.3mol分别投入到含0.1mol HCl的盐酸中,同温同压下产生气体的体积比是_____________________。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省绍兴市高一上学期阶段性考试化学试卷(解析版) 题型:填空题
已知钠能与水剧烈反应:2Na+2H2O=2NaOH+H2↑
(1)相同质量的Na,Mg,Al与过量的盐酸反应,在相同的状况下,三者置换出的H2的体积比是____________________________。
(2)相同物质的量的Na,Mg,Al与过量的盐酸反应,在相同状况下,三者置换出的H2的体积比是_________________________。
(3)Na,Mg,Al与过量的盐酸反应,在相同状况下产生的氢气的体积相等,则Na,Mg,Al三种金属的物质的量之比是__________________________。
(4)将Na,Mg,Al各0.3mol分别投入到含0.1mol HCl的盐酸中,同温同压下产生气体的体积比是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
我国多次成功发射了“神舟”载人飞船,为我国的航天事业写下了新的篇章。
(1)火箭升空时,由于与大气层的剧烈摩擦,产生高温,为了防止火箭温度过高,在火箭表面涂上一种特殊的涂料,该涂利的性质最可能的是(选填序号) ;
①在高温下不融化 ②在高温下可分解气化
③有强氧化性 ④见光易分解
(2)火箭用的燃料是液态的偏二甲肼和四氧化二氮,已知偏二甲肼含C、H、N三种元素,其中C、N两元素的质量分数分别为40.00%和46.67%,在相同状况下偏二甲肼的密度是H2的30倍,则偏二甲肼的分子式为 ;
(3)若0.1mol液态的偏二甲肼与液态N2O4完全反应,生成气态的N2、H20和CO2,同时放出![]() kJ热量,该反应的氧化剂是 (填化学式);
kJ热量,该反应的氧化剂是 (填化学式);
试写出该反应的热化学方程式:
这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是:
(4)假如用液态的偏二甲肼和液态氧作为燃料,那么该燃烧反应的化学方程式为:
;
(5)通常情况下N2O4气体和NO2气体可相互转化;N2O4(g)I(无色)![]() 2NO2(g) (红棕色)
2NO2(g) (红棕色)![]() 。下列说法错误的是(选填序号) 。
。下列说法错误的是(选填序号) 。
①N2O4和NO2互为同素异形体
②若反应在恒容的密闭容器中进行,升温时平衡混合气体颜色加深
③鉴别NO2气体和溴蒸汽可选用硝酸银溶液
④N2O4和NO2都是硝酸的酸酐
查看答案和解析>>
科目:高中化学 来源:期中题 题型:推断题
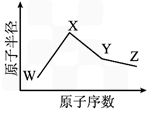
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com