
【题目】下列物质中,不属于合金的是( )
A. 硬铝 B. 黄铜 C. 水银 D. 钢铁
 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1
FeO(s)+CO(g) ΔH1,平衡常数为K1
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2
FeO(s)+H2(g) ΔH2,平衡常数为K2
在不同温度时K1、K2的值如下表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH,平衡常数为K,则ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g) ΔH,平衡常数为K,则ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g) ![]() CO(g)+H2O(g)是_________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是_________反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图1所示:
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图1所示:

①该条件下反应的平衡常数为___________;若铁粉足量,CO2的起始浓度为2.0 mol/L,则平衡时CO2的浓度为________mol/L。
②下列措施中能使平衡时CO物质的量百分数增大的是________(填序号)。
A.升高温度 B.增大压强
C.再充入一定量的CO2 D.再加入一定量铁粉
(3)对于可逆反应Fe(s)+CO2(g)![]() FeO(s)+CO(g),该反应的逆反应速率随时间变化的关系如图2。
FeO(s)+CO(g),该反应的逆反应速率随时间变化的关系如图2。
①从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是______。
A.升温 B.增大CO2浓度 C.使用催化剂
②如果在t3时从混合物中分离出部分CO,t4~t5时间段反应处于新平衡状态,请在图上画出t3~t5的v逆变化曲线_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( ) 
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2周期第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中反应制得:①3SiO2+6C+2N2![]() Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3![]() Si3N4+12HCl。则下列叙述正确的是
Si3N4+12HCl。则下列叙述正确的是
A. 反应②属于离子反应
B. 若制取等量的Si3N4,则反应①②转移电子数目必然相等
C. 反应①的氧化剂是N2
D. 反应①中氧化产物与还原产物物质的量之比为1∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关合理用药的下列说法中,错误的是( )
A. 对症下药是合理用药的首要原则
B. 能被充分、快速吸收而无刺激性的药物,可在饭前口服
C. 一种药物的用量,是经过严格的科学实验和大量的临床研究确定的
D. 因为青霉素能够杀菌,所以过期的青霉素仍然能够使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2NO2(g)![]() N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
A. 体积不变,增加NO2的量 B. 体积不变,增加N2O4的量
C. 体积不变,充入N2 D. 体积扩大到原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
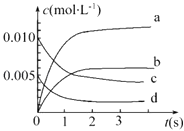
(1)上述反应在第5s时,NO的转化率为 .
(2)如图中表示NO2变化曲线的是 . 用O2表示0~2s内该反应的平均速率v= .
(3)能说明该反应已达到平衡状态的是 .
a.v(NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,

请写出N2和H2反应的热化学方程式:______________________________________________;
(2)若已知下列数据:
化学键 | H-H | N≡N |
键能/kJ mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能____________kJ mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1_______,△H________ (填“增大”、“减小、” “不变”)。
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1=akJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=bkJ·mol-1
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=_________kJ/mol (用含a、b的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com