
写出1---18号元素中符合下列条件的原子(离子)结构示意图:
①原子核外M电子层上有2个电子的原子;
②得到2个电子后,其电子层结构与Ne相同的离子;
③微粒带有一个单位的正电荷,核电荷数为11;
④微粒核外有18个电子,当失去1个电子时呈电中性;
⑤微粒不带电,其质数量为1
依次写出各微粒的结构示意图 : 、
、 、
科目:高中化学 来源:2014-2015学年河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.CH4分子的球棍模型:
B.Cl-离子的结构示意图: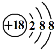
C.氟化钠的电子式: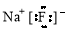
D.中子数为146、质子数为92 的铀原子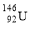
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高一上学期第一次月考化学试卷(解析版) 题型:填空题
(10分) KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其变化可表述为:
2KClO3 + 4HCl(浓) = 2 KCl + 2 ClO2↑ + Cl2↑ + 2 H2O
(1)用“双线桥法”标出电子转移的方向和数目。
(2)浓盐酸在反应中显示出来的性质是 (填编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1 mol Cl2,则转移的电子的数目为 ,标况下该反应产生气体体积为
(4)还原剂和还原产物物质的量之比
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.液态HCl不导电,所以HCl是非电解质
B.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
C.铜、石墨均导电,所以它们都是电解质
D.蔗糖在水溶液中或熔融时均不导电,所以是非电解质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.硫酸的摩尔质量是98g
B.1mol氧的质量等于16g
C.摩尔是一个基本物理量
D.12g 12C所含原子数称为阿伏加德罗常数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列物质既能由金属和酸反应获得,也能通过金属和氯气反应获得的是
A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高一上学期期中考试化学试卷(解析版) 题型:选择题
取100mL0.3mol/L硫酸和300mL0.25mol/L的硫酸溶液,混合后稀释到500 mL,则得到的混合溶液中氢离子的物质的量浓度为
A.0.21mol/L B.0.56mol/L C.0.42mol/L D.0.26mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省赣州市高一上学期第一次月考化学卷(解析版) 题型:填空题
松花蛋腌制配方有多种,但主要配料为生石灰(CaO)、纯碱和食盐。将一定比例的配料用水和黏土调制成糊状,敷于蛋上,密封保存,数日后即可食用。
(1)腌制松花蛋的配料用水调制时,发生的主要反应的化学方程式有(不考虑黏土中物质可能参与的反应)
。
(2)松花蛋外的糊状物经水溶解、过滤后,滤液中肯定大量含有的溶质为 和 ,可能含有的物质为Ca(OH)2或Na2CO3。
(3)某同学设计如下表所示实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
实验步骤 | 实验现象 | 结论 |
①取少量滤液,滴加适量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
若无白色沉淀 | 滤液中无Ca(OH)2 | |
②取少量滤液, 。 | 若出现 。 | 滤液中含Na2CO3 |
问题讨论:在什么情况下可以不必做实验②就可以得出结论? 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高二上学期期中化学(理)试卷(解析版) 题型:填空题
(共10分) 甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应Ⅰ:CO(g)+2H2(g)  CH3OH(g),△H1
CH3OH(g),△H1
反应Ⅱ:C02(g)+3H2(g)  CH30H(g)+ H2O(g),△H2
CH30H(g)+ H2O(g),△H2
下表所列数据是反应I在不同温度下的化学平衡常数(K):
温度 | 250℃ | 300℃ | 350℃ |
K | 2.O | 0.27 | 0.012 |
(1)在一定条件下将2 molCO和6molH2充入2L的密闭容器中发生反应I,5min后测得c(CO)=0.4 mol/L,计算此段时间的反应速率(用H2表示) mol/(L·min)。
(2)由表中数据判断△H1 0(填“>”、“<”或“=”)反应C02(g)+H2(g) CO(g)+H20(g)△H3= (用△H1和△H2表示)。
CO(g)+H20(g)△H3= (用△H1和△H2表示)。
(3)若容器容积不变,下列措施可提高反应Ⅰ中CO转化率的是 (选字母)。
a.充入CO,使体系总压强增大
b.将CH3OH(g)从体系中分离
e.充入He,使体系总压强增大
d.使用高效催化剂
(4)写出反应Ⅱ的化学平衡常数表达式:K= ;保持恒温恒容的条件下将反应Ⅱ的平衡体系各物质浓度均增加一倍,则化学平衡 (填“正向”、“逆向”或“不”)移动,平衡常数K (填“变大”、“变小”或“不变”)。
(5)这两种合成甲醇的方法比较,原子利用率较高的是 (填“Ⅰ”或“Ⅱ”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com