
| A. | pH=6的溶液一定呈酸性 | |
| B. | c(H+)水电离产生=c(OH-)水电离产生的溶液一定呈中性 | |
| C. | 使石蕊试液显红色的溶液一定呈酸性 | |
| D. | 强酸和强碱等物质的量混合后溶液一定呈中性 |
分析 A.pH=6的溶液不一定呈酸性,可能呈中性;
B.任何电解质水溶液中都存在c(H+)水电离产生=c(OH-)水电离产生,但存在c(H+)水电离产生=c(OH-)水电离产生的溶液不一定呈中性;
C.石蕊试液变色范围是5-8;
D.强酸和强碱等物质的量混合后溶液可能呈中性,也可能呈酸性或碱性.
解答 解:A.pH=6的溶液不一定呈酸性,可能呈中性,如95℃的水中存在c(H+)=c(OH-)=10-6 mol/L,溶液的pH=6且溶液呈中性,故A错误;
B.任何电解质水溶液中都存在c(H+)水电离产生=c(OH-)水电离产生,但存在c(H+)水电离产生=c(OH-)水电离产生的溶液不一定呈中性,可能呈酸性或碱性,故B错误;
C.石蕊试液变色范围是5-8,常温下pH<5的溶液能使石蕊试液变红色,为酸性溶液,故C正确;
D.强酸和强碱等物质的量混合后溶液可能呈中性,也可能呈酸性或碱性,如:元数相同的强酸强碱等物质的量的混合溶液呈中性,如果酸的元数大于碱的元数,二者等物质的量混合后溶液呈酸性,如果酸的元数小于碱的元数,二者等物质的量混合后溶液呈碱性,故D错误;
故选C.
点评 本题考查探究溶液酸碱性,为高频考点,侧重考查学生对溶液酸碱性及pH的理解与判断,在温度未知时不能根据溶液pH判断溶液酸碱性,易错选项是B.


科目:高中化学 来源: 题型:解答题
 某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 | |
| B. | 在河流入海处易形成沙洲 | |
| C. | 清晨,在茂密的树林中,常常可以看到枝叶间透过的一道道光柱 | |
| D. | 氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该星球表面温度很高 | |
| B. | 该星球表面温度很低 | |
| C. | 低温下稳定性CH2=CHOH>CH3CHO | |
| D. | 该反应中CH2=CHOH化学键断裂吸收能量大于CH3CHO化学键形成放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应是放热反应的可逆反应,升高温度v(正)>v(逆) | |
| B. | 升高温度或使用催化剂是通过增加活化分子百分数而使反应速率加快 | |
| C. | 勒夏特列原理只使用于可逆反应,不使用于溶解和弱电解质的电离 | |
| D. | △G=△H-T△S适合任意条件的化学反应进行的方向判据 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
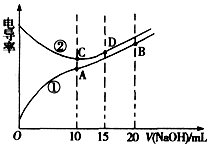
| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05 mol.L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C | |
| D. | D点溶液中:c(Cl-)=2c(OH-)-2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积/ml | 标准盐酸体积/ml | |
| 滴定前读数/ml | 滴定后读数/ml | ||
| 第一次 | 10.00 | 0.20 | 22.90 |
| 第二次 | 10.00 | 0.50 | 20.40 |
| 第三次 | 10.00 | 4.00 | 24.10 |
| 第四次 | 10.00 | 0.00 | 20.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com