
| 88×68.2% |
| 12 |
| 88×13.6% |
| 1 |
| 88-12×5-12 |
| 16 |
 ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大.A原子、C原子的L电子层中,都有两个未成对的电子,C、D同主族.E、F都是第四周期元素,E原子核外有4个未成对电子,F原子的外围电子排布式为3d104s1.请填空:
已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大.A原子、C原子的L电子层中,都有两个未成对的电子,C、D同主族.E、F都是第四周期元素,E原子核外有4个未成对电子,F原子的外围电子排布式为3d104s1.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| H2SO4 |
| NH3.H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、MnO2 CuO FeO |
| B、(NH4)2SO4 K2SO4 NH4Cl |
| C、AgNO3 KNO3 Na2CO3 |
| D、Na2CO3 CaCO3 K2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.8 | B、11.6 |
| C、23.2 | D、46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
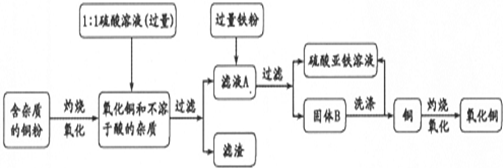
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用25ml量筒量取12.3ml盐酸;用托盘天平称取8.75g食盐 |
| B、用pH试纸测得某氯水的pH为2;用标准NaOH溶液滴定未知浓度的盐酸,用去NaOH溶液23.10ml |
| C、将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数大于15% |
| D、浓硝酸必须保存在棕色玻璃瓶中;钠必须保存在煤油中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com